题目内容
25mL浓度为0.04mol?L-1的Na2SO3溶液恰好与20mL浓度为0.02mol?L-1的KRO4溶液完全反应.已知Na2SO3被KRO4氧化为Na2SO4,则R元素在还原产物中的化合价为( )
| A、+2 | B、+3 | C、+4 | D、+5 |
考点:氧化还原反应的计算
专题:
分析:n(Na2SO3)=0.04mol/L×0.025L=0.001mol,n(KRO4)=0.02mol/L×0.02L=0.0004mol,KRO4和Na2SO3发生氧化还原反应生成Na2SO4,根据原子守恒计算R元素在还原产物中的化合价,据此分析解答.
解答:
解:n(Na2SO3)=0.04mol/L×0.025L=0.001mol,n(KRO4)=0.02mol/L×0.02L=0.0004mol,KRO4和Na2SO3发生氧化还原反应生成Na2SO4,设R元素在还原产物中的化合价为x,根据转移电子守恒得0.001mol×(6-4)=0.0004mol×(7-x),x=+2,故选A.
点评:本题考查氧化还原反应的计算,侧重考查学生分析能力、计算能力,明确转移电子守恒是解本题关键,题目难度不大.

练习册系列答案
相关题目
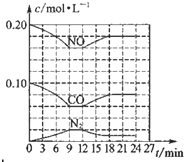 将0.20mol NO和0.1mol CO充入一个容积恒定为1L的密闭容器中发生反应:2NO(g)+2CO(g)═N2(g)+2CO2(g)△H<0在不同条件下,反应过程中部分物质的浓度变化如图所示.下列说法正确的是( )
将0.20mol NO和0.1mol CO充入一个容积恒定为1L的密闭容器中发生反应:2NO(g)+2CO(g)═N2(g)+2CO2(g)△H<0在不同条件下,反应过程中部分物质的浓度变化如图所示.下列说法正确的是( )| A、容器内的压强不发生变化说明该反应达到平衡 |
| B、当向容器中再充入0.20 mol NO时,平衡向正反应方向移动,K增大 |
| C、第12 min时改变的反应条件为减小压强 |
| D、向该容器内充入He气,容器内气体压强增大,所以反应速率增大 |
下列反应中,有沉淀产生且不会消失的是( )
| A、向NaOH溶液中逐滴滴入Fe2(SO4)3溶液直至过量 |
| B、将NaOH溶液逐滴滴入AlCl3溶液中,直至过量 |
| C、向AlCl3溶液中逐滴滴入稀硫酸 |
| D、将氨水逐滴滴入硝酸银溶液中,直至过量 |
某探究小组利用丙酮的溴代反应(CH3COCH3+Br2
CH3COCH2Br+HBr)来研究反应物浓度与反应速率的关系.反应速率v(Br2)通过测定溴的颜色消失所需的时间来确定.在一定温度下,获得如下实验数据:
分析实验数据所得出的结论不正确的( )
| HCl |
| 实 验 序 号 | 初始浓度c/mol?L-1 | 溴颜色消失 所需时间t/s | ||
| CH3COCH3 | HCl | Br2 | ||
| ① | 0.80 | 0.20 | 0.0010 | 290 |
| ② | 1.60 | 0.20 | 0.0010 | 145 |
| ③ | 0.80 | 0.40 | 0.0010 | 145 |
| ④ | 0.80 | 0.20 | 0.0020 | 580 |
| A、增大c(Br2),v(Br2)增大 |
| B、实验②和③的v(Br2)相 |
| C、增c(HCl),v(Br2)增大 |
| D、增大c(CH3COCH3),v(Br2)增大 |
下列叙述正确的是( )
| A、同温同压下,物质的物质的量相等,其体积一定相同 |
| B、等体积的二氧化碳和一氧化碳所含的分子数一定相等 |
| C、1L氮气一定比1L氧气的质量小 |
| D、相同条件下的一氧化碳气体和氮气,若体积相等,则质量一定相等 |
A、B、C、D、E是同一周期的五种主族元素,A与B的最高氧化物对应的水化物呈碱性,且碱性B>A;C和D的气态氢化物稳定性为C>D;E是这五种元素中原子半径最小的元素,则它们的原子序数由小到大的顺序为( )
| A、ABCDE |
| B、CDABE |
| C、BADCE |
| D、ECDBA |
0.75molRO32- 共有30mol电子,则R在元素周期表中的位置是( )
| A、.第二周期ⅤA族 |
| B、.第三周期ⅣA族 |
| C、.第二周期ⅥA族 |
| D、.第三周期Ⅶ族 |