题目内容
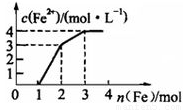
现有含Fe(NO3)3、Cu(NO3)2、HNO3 的某稀溶液,若向其中逐步加入铁粉,溶液中Fe2+ 浓度与加入铁粉的物质的量之间的关系如图所示,则该溶液中Fe(NO3)3、Cu(NO3)2、HNO3物质的量浓度之比为

A.1∶1∶1 B.1∶1∶4 C.3∶3∶8 D.1∶3∶1
【答案】
B
【解析】由三者的氧化性强弱,可知加入铁粉依次发生如下三个反应:
Fe+4HNO3=Fe(NO3)3+NO+2H2O
2Fe(NO3)3+Fe=3Fe(NO3)2
Cu(NO3)2 +Fe = Fe(NO3)2 +Cu
各方程式中铁粉均为 1 mol,可推知参加反应的Fe(NO3)3、Cu(NO3)2、HNO3分别为2 mol、1 mol、4 mol,故原溶液中三者的物质的量依次为1 mol、1 mol、4 mol。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目