题目内容
15.设NA为阿伏加德罗常数的值.下列说法正确的是( )| A. | 80mL 10mol/L的浓盐酸与足量的MnO2加热反应,产生Cl2分子数为0.2NA | |
| B. | 25g质量分数为68%的H2O2水溶液中含氧原子数目为NA | |
| C. | 1L 1mol/L的Fe2(SO4)3溶液中含有的SO42-离子数为3NA | |
| D. | 常温常压下,等质量的CO和N2中含有的原子数目均为2NA |
分析 A.稀盐酸不反应;
B.双氧水的水溶液中,双氧水分子和水分子都含有氧原子;
C.1L 1mol/L的Fe2(SO4)3溶液含有Fe2(SO4)3为1mol;
D.氮气和一氧化碳的摩尔质量都是28g/mol,一个分子中含有2个原子.
解答 解:A.随反应进行,盐酸浓度减小,稀盐酸不反应,产生Cl2分子数小于0.2NA,故A错误;
B.双氧水和都含有氧原子,25g质量分数68%的H2O2水溶液中含氧原子数目大于NA,故B错误;
C.1L 1mol/L的Fe2(SO4)3溶液含有Fe2(SO4)3为1mol,含有的SO42-离子数为3NA,故C正确;
D.氮气和一氧化碳的摩尔质量都是28g/mol,等质量的CO和N2中含有的原子数目均为2NA,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的分析应用,题目难度中等,明确物质的结构及反应的条件是解题关键,注意熟练掌握物质的量与摩尔质量、阿伏伽德罗常数等物理量之间的关系.

练习册系列答案
 优加精卷系列答案
优加精卷系列答案
相关题目
3.表为元素周期表的一部分,其中X、Y、Z、W为短周期元素,W元素的核电荷数为X元素的2倍.下列说法正确的是( )
| X | ||
| Y | Z | W |
| T |
| A. | X、W、Z元素的原子半径依次减小 | |
| B. | Y、Z、W元素在自然界中均不能以游离态存在,它们的最高价氧化物的水化物的酸性依次递增 | |
| C. | YX2晶体熔化、液态WX3气化均需克服分子间作用力 | |
| D. | 根据元素周期律,可以推测T2X3具有氧化性和还原性 |
10.常温下已知两种一元弱酸HX和HY,如果向NaX溶液中通CO2气体,只能生成HX和NaHCO3;往NaY溶液中通入CO2则生成HY和Na2CO3.有关叙述正确的是( )
| A. | 结合H+的能力:Y>CO${\;}_{3}^{2-}$>X>HCO${\;}_{3}^{-}$ | |
| B. | 三种酸的电离常数Ki(HX)>Ki(HY)>Ki(H2CO3) | |
| C. | 溶液碱性:NaX>Na2CO3>NaY>NaHCO3 | |
| D. | NaX溶液中通入足量CO2后的离子浓度:c(Na+)>c(HCO${\;}_{3}^{-}$)>c (X)>c(OH)>c(H+) |
20.实验是化学研究的基础,下列关于各实验装置图中叙述,正确的是( )
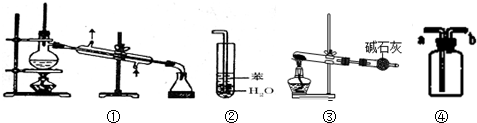

| A. | 装置①常用于分离互不相溶的液体混合物 | |
| B. | 装置②可用于吸收氨气,防止倒吸 | |
| C. | 以KClO3 为原料,装置③可用于制备少量O2 | |
| D. | 装置④a进口可收集H2、CO 等气体 |
7.已知M(C8Hl602)发生水解反应可生成A、B两种化合物,在一定条件下A可转化为B,则所有A、B反应生成的物质有( )
| A. | 2种 | B. | 4种 | C. | 6种 | D. | 8种 |
4.下列有关化学用于表示正确的是( )
| A. | Ba (OH)2溶液与过量NaHCO3溶液混合离子方程式:Ba2++OH-+HCO3-═BaCO3↓+H2O | |
| B. | Na+的结构示意图: | |
| C. | 原子核内有10个中子的氧原子:${\;}_{8}^{18}$O | |
| D. | 氢氧化铁的电离方程式:Fe(OH)3═Fe3++3OH- |
5.用试纸检验气体是一种重要的实验方法.下列试纸的选用以及对应的现象、结论都正确的一项是( )
| A. | 用干燥的pH试纸检验CO2 | |
| B. | 用干燥的红色石蕊试纸检验NH3 | |
| C. | SO2能使湿润的品红试纸褪色 | |
| D. | 能使湿润的淀粉碘化钾试纸变蓝的气体一定是氯气 |
 .
.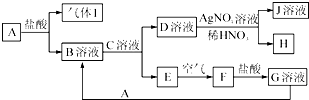 已知A~J都是中学化学中的常见物质,其中A、I为单质,E、H是白色沉淀,F为红褐色沉淀,J溶液的焰色反应(透过蓝色的钴玻璃观察)呈紫色,各物质之间的转化关系如图所示.
已知A~J都是中学化学中的常见物质,其中A、I为单质,E、H是白色沉淀,F为红褐色沉淀,J溶液的焰色反应(透过蓝色的钴玻璃观察)呈紫色,各物质之间的转化关系如图所示. .
.