题目内容
 将镉(Cd)浸在氯化钴(CoCl2)溶液中,发生反应的离子方程式为:Co2+(aq)+Cd(s)=Co(s)+Cd2+(aq)(aq表示溶液),如将该反应设计为如右图的原电池,则下列说法一定错误的是( )
将镉(Cd)浸在氯化钴(CoCl2)溶液中,发生反应的离子方程式为:Co2+(aq)+Cd(s)=Co(s)+Cd2+(aq)(aq表示溶液),如将该反应设计为如右图的原电池,则下列说法一定错误的是( )| A、Cd作负极,Co作正极 |
| B、原电池工作时,电子从负极沿导线流向正极 |
| C、根据阴阳相吸原理,盐桥中的阳离子向负极(甲池)移 动 |
| D、甲池中盛放的是CdCl2溶液,乙池中盛放的是CoCl2溶液 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A.失电子的金属作负极、发生还原反应的电极作正极;
B.放电时,电子从负极沿导线流向正极;
C.盐桥中阳离子向正极区域移动、阴离子向负极区域移动;
D.含有Cd2+的溶液为负极区域电解质溶液,含有Co2+的溶液为正极区域电解质溶液.
B.放电时,电子从负极沿导线流向正极;
C.盐桥中阳离子向正极区域移动、阴离子向负极区域移动;
D.含有Cd2+的溶液为负极区域电解质溶液,含有Co2+的溶液为正极区域电解质溶液.
解答:
解:A.反应Co2+(aq)+Cd(s)=Co(s)+Cd2+(aq)(aq表示溶液)中Co得电子发生还原反应,则Co作正极、Cd作负极,故A正确;
B.放电时,电子从负极Cd沿导线流向正极Co,故B正确;
C.盐桥中阳离子向正极极区域乙移动、阴离子向负极区域甲移动,故C错误;
D.甲中失电子发生氧化反应,电解质溶液为CdCl2溶液,乙池中盛放的是CoCl2溶液,故D正确;
故选C.
B.放电时,电子从负极Cd沿导线流向正极Co,故B正确;
C.盐桥中阳离子向正极极区域乙移动、阴离子向负极区域甲移动,故C错误;
D.甲中失电子发生氧化反应,电解质溶液为CdCl2溶液,乙池中盛放的是CoCl2溶液,故D正确;
故选C.
点评:本题考查了原电池原理,明确正负极上发生的电极反应及元素化合价变化是解本题关键,再结合离子移动方向来分析解答,离子移动方向的判断为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
化学环境、材料、信息、能源关系密切,下列说法不正确的是( )
| A、利用催化设施,可以将汽车尾气中CO和NO转化为无害气体 |
| B、在入海口的钢闸门上装一定数量的铜块可防止闸门被腐蚀 |
| C、先通入氯气,再加入硫酸亚铁处理水,能达到消毒杀菌和除去悬浮杂质的目的 |
| D、半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是硅 |
下列关于常温下电解质溶液的叙述中,正确的是( )
| A、碳酸氢铵溶液和足量氢氧化钠溶液混合,反应的离子方程式为:HCO3-+OH-═CO32-+H2O |
| B、25℃时,pH=8的0.1mol?L-1NaX溶液中由水电离出的c(OH-)=1×10-8mol?L-1 |
| C、等物质的量浓度的NH4Cl溶液和NH3?H2O溶液中,c(NH4+)前者小于后者 |
| D、等物质的量浓度、等体积的氨水和盐酸混合后,c(H+)+c(NH4+)=c(Cl-)+c(OH-) |
下列实验、现象与结论不一致的是( )
| 选项 | A | B | C | D |
| 实验 | 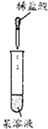 | 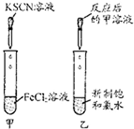 |  | 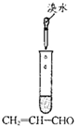 |
| 现象 | 出现白色沉淀 | 甲、乙中溶液均未变红 | 苯中不褪色,甲苯在褪色 | 溶液褪色 |
| 结论 | 原溶液可能含Ag+或SiO32- | 氯水可能氧化SCN- | 甲苯中甲基易被氧化 | 可证明分子中含碳碳双建 |
| A、A | B、B | C、C | D、D |
下列物质中不能由金属与盐酸直接反应制得的是( )
| A、氯化镁 | B、氯化锌 |
| C、氯化铁 | D、氯化铝 |
用NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A、32g氧气和28g CO和N2的混合气体,含为原子数目相等 |
| B、等物质的量浓度的盐酸和硫酸,H+的物质的量浓度相等 |
| C、在常温常压下,11.2L氯气的分子数为0.5NA |
| D、把40g NaOH固体溶于1L水中,所得NaOH溶液的物质的量浓度为1mol?L-1 |