题目内容
13.实验室可以用高锰酸钾固体和浓盐酸反应制取氯气,反应的化学方程武如下:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O
(l)用单线桥法标出电子转移的方向和数目:
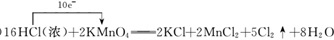 .
.(2)该反应中的氧化剂与还原剂的物质的量之比是1:5.
(3)KMnO4的氧化性比Cl2的氧化性强(填“强”或“弱”).
(4)反应中每转移2mol电子,产生的Cl2为22.4L(标准状况).
分析 (1)反应中锰元素全部被还原,锰元素化合价由+7价降低为+2价,氯元素化合价由HCl中的-1升高为氯气中的0价,反应电子转移的数目为10e-;
(2)反应中2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O,高锰酸钾是氧化剂,浓盐酸部分是还原剂,由此分析解答;
(3)氧化剂的氧化性强于氧化产物的氧化性,所以KMnO4的氧化性比Cl2的氧化性强;
(4)由反应方程式可知:每转移10mol的电子,产生氯气为:5mol,所以反应中每转移2mol电子,产生的Cl2为1mol,由此解答.
解答 解:(1)反应中锰元素全部被还原,锰元素化合价由+7价降低为+2价,氯元素化合价由HCl中的-1升高为氯气中的0价,反应电子转移的数目为10e-,所以电子转移的方向和数目为: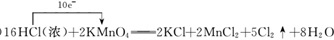 ,故答案为:
,故答案为: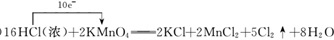 ;
;
(2)反应中2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O,高锰酸钾是氧化剂,浓盐酸部分是还原剂,16mol盐酸中只有10mol的氯的化合价变化,充当还原剂,所以氧化剂与还原剂的物质的量之比是1:5,故答案为:1:5;
(3)氧化剂的氧化性强于氧化产物的氧化性,所以KMnO4的氧化性比Cl2的氧化性强,故答案为:强;
(4)由反应方程式可知:每转移10mol的电子,产生氯气为:5mol,所以反应中每转移2mol电子,产生的Cl2为1mol,所以标况下的体积为:22.4L,故答案为:22.4L.
点评 本题考查氧化还原反应基本概念与计算,难度不大,(3)可以先计算参加反应的HCl,再根据方程式计算生成的氯气,也可利用电子转移守恒计算,根据情况选择.

练习册系列答案
相关题目
1.下列对有机化合物的分类正确的是( )
| A. | 乙烯、苯、环己烷属于脂肪烃 | B. | 苯、环己烷属于芳香烃 | ||
| C. | 乙烯、乙炔属于烯烃 | D. | 环戊烷、环己烷属于环烷烃 |
8.下列物质不属于有机合成材料的是( )
| A. | 塑料瓶 | B. | 不锈钢 | C. | 涤纶布料 | D. | 合成纤维 |
18.以下转化不能通过一步反应实现的是( )
| A. | Al2O3→Al(OH)3 | B. | SiO2→SiF4 | C. | Fe→FeCl2 | D. | Na→NaOH |
3.在一定温度下的固定容积的密闭容器中,当下列物理量不再变化时,表明反应:A(s)+2B(g)?C(g)+D(g)已达平衡的是( )
| A. | 混合气体的压强 | B. | 气体的总物质的量 | ||
| C. | 消耗1摩尔A同时生成1摩尔D | D. | 混合气体的密度 |
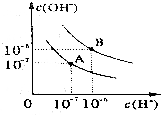 已知水在25℃和95℃时,其电离平衡曲线如图所示:
已知水在25℃和95℃时,其电离平衡曲线如图所示: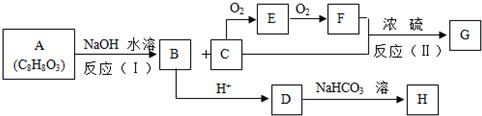
 ,E:HCHO,H:
,E:HCHO,H: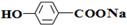 G:HCOOCH3,.
G:HCOOCH3,. .
.