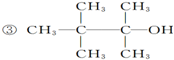
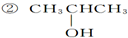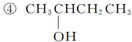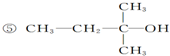题目内容
某有机物A的相对分子质量为60.为进一步测定A的化学式,现取6.0gA完全燃烧,得到二氧化碳和水蒸气.将产物先后通过足量的浓硫酸和碱石灰,两者分别增重3.6g和8.8g (假设每步反应完全).
(1)该有机物的最简式是 ,分子式是 ;
(2)该有机物能与碳酸氢钠反应产生二氧化碳,推断该有机物的结构简式是 ;
(3)该有机物与碳酸氢钠反应的离子方程式是 .
(4)该有机物不具有的性质是
A.与金属钠反应 B.与稀硫酸反应
C.发生酯化反应D.使酸性高锰酸钾溶液褪色.
(1)该有机物的最简式是
(2)该有机物能与碳酸氢钠反应产生二氧化碳,推断该有机物的结构简式是
(3)该有机物与碳酸氢钠反应的离子方程式是
(4)该有机物不具有的性质是
A.与金属钠反应 B.与稀硫酸反应
C.发生酯化反应D.使酸性高锰酸钾溶液褪色.
考点:有机物的推断
专题:有机物的化学性质及推断
分析:浓硫酸增重3.6g为水的质量,其物质的量为
=0.2mol,n(H)=0.4mol,m(H)=0.4mol×1g/mol=0.4g,碱石灰增重8.8g为二氧化碳的质量,其物质的量为
=0.2mol,n(C)=0.2mol,m(C)=0.2mol×12g/mol=2.4g,故有机物中m(O)=6g-0.4g-2.4g=3.2g,则n(O)=
=0.2mol,故该有机物最简式为CH2O,有机物相对分子质量为60,故有机物分子式为C2H4O2,该有机物能与碳酸氢钠反应产生二氧化碳,则该有机物结构简式为CH3COOH,据此解答.
| 3.6g |
| 18g/mol |
| 8.8g |
| 44g/mol |
| 3.2g |
| 16g/mol |
解答:
解:(1)浓硫酸增重3.6g为水的质量,其物质的量为
=0.2mol,n(H)=0.4mol,m(H)=0.4mol×1g/mol=0.4g,碱石灰增重8.8g为二氧化碳的质量,其物质的量为
=0.2mol,n(C)=0.2mol,m(C)=0.2mol×12g/mol=2.4g,故有机物中m(O)=6g-0.4g-2.4g=3.2g,则n(O)=
=0.2mol,则n(C):n(H):n(O)=0.2mol:0.4mol:0.2mol=1:2:1,故该有机物最简式为CH2O,有机物相对分子质量为60,故有机物分子式为C2H4O2,故答案为:CH2O;C2H4O2;
(2)该有机物能与碳酸氢钠反应产生二氧化碳,含有羧基,则该有机物结构简式为CH3COOH,故答案为:CH3COOH;
(3)该有机物与碳酸氢钠反应的离子方程式是:CH3COOH+HCO3-=CH3COO-+H2O+CO2↑,故答案为:CH3COOH+HCO3-=CH3COO-+H2O+CO2↑;
(3)有机物结构简式为CH3COOH,能与钠反应,能发生酯化反应,不能与稀硫酸、酸性高锰酸钾溶液反应,故选:BD.
| 3.6g |
| 18g/mol |
| 8.8g |
| 44g/mol |
| 3.2g |
| 16g/mol |
(2)该有机物能与碳酸氢钠反应产生二氧化碳,含有羧基,则该有机物结构简式为CH3COOH,故答案为:CH3COOH;
(3)该有机物与碳酸氢钠反应的离子方程式是:CH3COOH+HCO3-=CH3COO-+H2O+CO2↑,故答案为:CH3COOH+HCO3-=CH3COO-+H2O+CO2↑;
(3)有机物结构简式为CH3COOH,能与钠反应,能发生酯化反应,不能与稀硫酸、酸性高锰酸钾溶液反应,故选:BD.
点评:本题考查有机物推断、羧酸的性质等,关键是计算确定有机物的分子式,难度不大.

练习册系列答案
 优加精卷系列答案
优加精卷系列答案
相关题目