题目内容
4.可逆反应2Cl2(g)+2H2O(g)?4HCl(g)+O2 (g)△H>0,在一定条件下达到平衡后,分别采取下列措施,试回答:(填“增大”、“减小”、或“不变”)(1)降低温度,Cl2的转化率减小,v正减小
(2)保持容器体积不变,加入He,则HCl的物质的量不变
(3)保持容器的压强不变,加入He,则 O2的体积分数增大
(4)若恒温恒容,反应从Cl2和H2O开始至平衡,在这个变化过程中,平均相对分子质量减小.
(5)加入催化剂,则O2的物质的量不变.
分析 (1)降低温度,平衡逆移,Cl2的转化率减小;v正减小;
(2)保持容器体积不变,加入He,对反应无影响,所以HCl的物质的量不变;
(3)保持容器压强不变,加入He,体积变大,反应物所占分压减小,平衡正移,则O2的体积分数增大;
(4)若温度和体积不变,反应从Cl2和H2O开始至平衡,在这个变化过程中,容器的体积不变,气体的总质量也不变,气体总物质的量增大,所以相对分子质量减小;
(5)加入催化剂,影响化学反应速率但不影响化学平衡,所以O2的物质的量不变.
解答 解:(1)该反应的正方向为吸热反应,所以降低温度,平衡逆移,Cl2的转化率 减小;v正减小;故答案为:减小;减小;
(2)保持容器体积不变,加入He,容器体积不变,各物质的浓度不变,所以对反应无影响,所以HCl的物质的量不变,故答案为:不变;
(3)保持容器压强不变,加入He,体积变大,反应物所占分压减小,平衡正移,则O2的体积分数增大;故答案为:增大;
(4)若温度和体积不变,反应从Cl2和H2O开始至平衡,在这个变化过程中,容器的体积不变,气体的总质量也不变,$\overline{M}$=$\frac{m}{n}$,气体总物质的量增大,所以相对分子质量减小;
故答案为:减小;
(5)加入催化剂,影响化学反应速率但不影响化学平衡,所以O2的物质的量不变,故答案为:不变.
点评 本题考查了温度、压强对化学平衡的影响,注意平衡移动对总物质的量、平均分子量的影响,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
15.下列各组物质之间的化学反应,反应产物一定为纯净物的是( )
| A. | CH2=CH2+Br2 | B. | CH2=CH-CH2-CH3+HCl | ||
| C. | CH3-CH=CH2+H2O | D. | nCH2=CH-CH3 |
15.一定量的CO2与足量的碳在体积可变的恒压密闭容器中发生反应:C(s)+CO2(g)?2CO(g),反应平衡时,体系中气体体积分数与温度的关系如图所示.下列说法正确的是( )
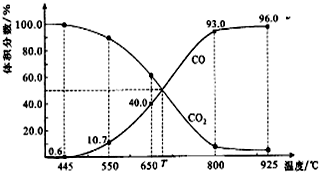

| A. | 550℃时,若充入惰性气体,v正,v逆均减小,平衡不移动 | |
| B. | 650℃时,反应达平衡后CO2的转化率为25.0% | |
| C. | T℃时,若充入等体积的CO2和CO,平衡向逆反应方向移动 | |
| D. | 该反应为吸热反应 |
19.五种短周期元素在周期表中的相对位置如下所示,其中Z元素原子核外电子总数是其最外层电子数的3倍.
请按要求回答下列问题:
(1)X元素名称碳,W的离子结构示意图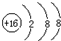 ;
;
(2)元素Z位于周期表中的位置是第三周期第VA族;
(3)元素Z可以形成多种单质,请任意写出一种常见单质的名称白磷或红磷;
(4)Y的最高价氧化物的化学式为N2O5;M的最高价氧化物水化物名称为高氯酸;
(5)Z、W、M三种元素中,原子半径最大的是P(填元素符号);这三者与氢元素形成的化合物中,最稳定的是HCl(填:氢化物的化学式),它的电子式为 ;
;
(6)X与M可形成XM4型化合物,是一种常见的溶剂,其中的化学键类型是共价键(填:“离子键”或“共价键”)
(7)W的氧化物有两种A和B,已知在某一定条件下,A和B能同时相互转化.则在该条件下A不能完全转化为B(填:“能”或“不能”)
| X | Y | ||
| Z | W | M |
(1)X元素名称碳,W的离子结构示意图
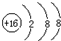 ;
;(2)元素Z位于周期表中的位置是第三周期第VA族;
(3)元素Z可以形成多种单质,请任意写出一种常见单质的名称白磷或红磷;
(4)Y的最高价氧化物的化学式为N2O5;M的最高价氧化物水化物名称为高氯酸;
(5)Z、W、M三种元素中,原子半径最大的是P(填元素符号);这三者与氢元素形成的化合物中,最稳定的是HCl(填:氢化物的化学式),它的电子式为
 ;
;(6)X与M可形成XM4型化合物,是一种常见的溶剂,其中的化学键类型是共价键(填:“离子键”或“共价键”)
(7)W的氧化物有两种A和B,已知在某一定条件下,A和B能同时相互转化.则在该条件下A不能完全转化为B(填:“能”或“不能”)
16.Ⅰ.高炉炼铁是冶炼铁的主要方法,发生的主要反应为
Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g)△H
(1)已知:Fe2O3(s)+3C(石墨,s)=2Fe(s)+3CO(g)△H1
C(石墨,s)+CO2(g)=2CO(g)△H2
则△H=△H1-3△H2(用含△H1、△H2代数式表示)
(2)在T℃时,该反应的平衡常数K=64,在2L恒容密闭容器甲和乙中,分别按表所示加入物质,反应经过一段时间后达到平衡.
①甲容器中CO的平衡转化率为60%.
②下列说法正确的是B(填字母).
A.若容器压强恒定,反应达到平衡状态
B.若容器内气体密度恒定,反应达到平衡状态
C.甲容器中CO的平衡转化率大于乙的
D.增加Fe2O3就能提高CO的转化率
II.利用空气催化氧化法制取联氨,其有关物质的转化如图1所示(R1、R2代表烃基).
①在图1示的转化中,化合价不变的一种元素是氢或H.
②反应中当有1mol NH3转化为N2H4时,保持溶液中酮的物质的量不变,需要消耗O2的物质的量为0.25mol.
③在温度一定和不补加溶液的条件下,缓慢通入NH3、O2混合气体,并充分搅拌.欲使生成的N2H4中不含NH3,可采取的措施有增大混合气体中氧气的含量.
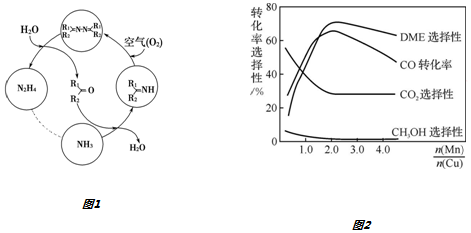
Ⅲ.采用一种新型的催化剂(主要成分是Cu-Mn的合金),利用CO和H2制备二甲醚(DME).观察如图2回答问题:催化剂中$\frac{n(Mn)}{n(Cu)}$约为2.0时最有利于二甲醚的合成.
Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g)△H
(1)已知:Fe2O3(s)+3C(石墨,s)=2Fe(s)+3CO(g)△H1
C(石墨,s)+CO2(g)=2CO(g)△H2
则△H=△H1-3△H2(用含△H1、△H2代数式表示)
(2)在T℃时,该反应的平衡常数K=64,在2L恒容密闭容器甲和乙中,分别按表所示加入物质,反应经过一段时间后达到平衡.
| Fe2O3 | CO | Fe | CO2 | |
| 甲/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| 乙/mol | 1.0 | 1.5 | 1.0 | 1.0 |
②下列说法正确的是B(填字母).
A.若容器压强恒定,反应达到平衡状态
B.若容器内气体密度恒定,反应达到平衡状态
C.甲容器中CO的平衡转化率大于乙的
D.增加Fe2O3就能提高CO的转化率
II.利用空气催化氧化法制取联氨,其有关物质的转化如图1所示(R1、R2代表烃基).
①在图1示的转化中,化合价不变的一种元素是氢或H.
②反应中当有1mol NH3转化为N2H4时,保持溶液中酮的物质的量不变,需要消耗O2的物质的量为0.25mol.
③在温度一定和不补加溶液的条件下,缓慢通入NH3、O2混合气体,并充分搅拌.欲使生成的N2H4中不含NH3,可采取的措施有增大混合气体中氧气的含量.

Ⅲ.采用一种新型的催化剂(主要成分是Cu-Mn的合金),利用CO和H2制备二甲醚(DME).观察如图2回答问题:催化剂中$\frac{n(Mn)}{n(Cu)}$约为2.0时最有利于二甲醚的合成.
 请回答下列问题:
请回答下列问题: