题目内容
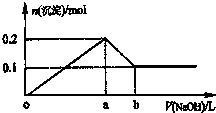 在AlCl3和MgCl2的混合溶液中,逐滴加入NaOH溶液直至过量,理论上,加入NaOH的体积和所得沉淀的物质的量的示意图如下,b处NaOH的体积为1L,则下列判断正确的是( )
在AlCl3和MgCl2的混合溶液中,逐滴加入NaOH溶液直至过量,理论上,加入NaOH的体积和所得沉淀的物质的量的示意图如下,b处NaOH的体积为1L,则下列判断正确的是( )| A、混合溶液中Al3+的物质的量为0.1mol |
| B、NaOH的浓度为0.5 mol/L |
| C、在b点处溶液中的溶质只有NaAlO2 |
| D、图中线段oa:ab=4:1 |
考点:离子方程式的有关计算
专题:计算题
分析:AlCl3和MgCl2的混合溶液中,逐滴加入NaOH溶液,发生反应生成氢氧化铝、氢氧化镁沉淀,加入aLNaOH溶液时,沉淀达最大值共0.2mol,此时溶液为NaCl溶液,继续滴加NaOH溶液直至过量,氢氧化铝与NaOH反应逐渐溶解,在bL时,即再继续滴加NaOH溶液(b-a)L时,氢氧化铝完全溶解,沉淀为氢氧化镁0.1mol,溶液为NaCl、NaAlO2溶液.
解答:
解:A、根据图示信息和Al原子守恒有:n(NaAlO2)=n(AlCl3)=n[Al(OH)3]=0.1mol,故A正确;
B、在bL时,溶液为NaCl、NaAlO2溶液,由图象可知:n[Al(OH)3]=0.1mol,n(Mg(OH)2]=0.1mol,根据Mg原子守恒有n(MgCl2)=n(Mg(OH)2]=0.1mol,根据Al原子守恒有n(NaAlO2)=n(AlCl3)=n[Al(OH)3]=0.1mol,由Cl原子守恒有n(Cl)=n(NaCl)=2n(MgCl2)+3n(AlCl3)=2×0.1mol+3×0.1mol=0.5mol,由Na原子守恒有n(NaOH)=n(NaCl)+n(NaAlO2)=0.5mol+0.1mol=0.6mol,所以c(NaOH)=
=0.6mol/L,故B错误;
C、在bL时,即再继续滴加NaOH溶液(b-a)L时,氢氧化铝完全溶解,沉淀为氢氧化镁0.1mol,溶液为NaCl、NaAlO2溶液,故C错误;
D、加入aLNaOH溶液时,沉淀达最大值共0.2mol,由反应方程式可知,此时溶液为NaCl溶液,在bL时,即再继续滴加NaOH溶液(b-a)L时,氢氧化铝与NaOH恰好反应,氢氧化铝完全溶解,沉淀为氢氧化镁0.1mol,溶液为NaCl、NaAlO2溶液,所以两部分NaOH溶液的体积之比等于消耗的NaOH的物质的量之比,即为n(NaCl)与n(NaAlO2)之比,故oa:ab=a:(b-a)=0.5mol:0.1mol=5:1,故D错误.
故选A.
B、在bL时,溶液为NaCl、NaAlO2溶液,由图象可知:n[Al(OH)3]=0.1mol,n(Mg(OH)2]=0.1mol,根据Mg原子守恒有n(MgCl2)=n(Mg(OH)2]=0.1mol,根据Al原子守恒有n(NaAlO2)=n(AlCl3)=n[Al(OH)3]=0.1mol,由Cl原子守恒有n(Cl)=n(NaCl)=2n(MgCl2)+3n(AlCl3)=2×0.1mol+3×0.1mol=0.5mol,由Na原子守恒有n(NaOH)=n(NaCl)+n(NaAlO2)=0.5mol+0.1mol=0.6mol,所以c(NaOH)=
| 0.6mol |
| 1L |
C、在bL时,即再继续滴加NaOH溶液(b-a)L时,氢氧化铝完全溶解,沉淀为氢氧化镁0.1mol,溶液为NaCl、NaAlO2溶液,故C错误;
D、加入aLNaOH溶液时,沉淀达最大值共0.2mol,由反应方程式可知,此时溶液为NaCl溶液,在bL时,即再继续滴加NaOH溶液(b-a)L时,氢氧化铝与NaOH恰好反应,氢氧化铝完全溶解,沉淀为氢氧化镁0.1mol,溶液为NaCl、NaAlO2溶液,所以两部分NaOH溶液的体积之比等于消耗的NaOH的物质的量之比,即为n(NaCl)与n(NaAlO2)之比,故oa:ab=a:(b-a)=0.5mol:0.1mol=5:1,故D错误.
故选A.
点评:理清反应的整个过程,问题即可解决,即可利用方程式也可根据关系式,本题采取原子守恒计算,难度较大.

练习册系列答案
相关题目
某气体混合物由H2、N2、CO和CH4中的一种或两种组成,将该混合气体点燃后的产物依次通过浓H2SO4和NaOH溶液,结果两溶液的质量均有增加.则该混合气体的组成不可能是( )
| A、N2和CO |
| B、H2和CO |
| C、CH4 |
| D、H2和CH4 |
水由于受到有机物污染而造成富营养化,使水中鱼类大批死亡,鱼类死亡是因为( )
| A、藻类大量繁殖,抢走了鱼类的营养 |
| B、水中缺氧,窒息而死 |
| C、水中氧气过多 |
| D、水中含有有毒的金属元素过多 |
下列试剂中,用来检验亚硫酸钠是否被氧化,较为合理的是( )
| A、氯化钡溶液和盐酸 |
| B、硝酸钡溶液和硝酸 |
| C、氢氧化钡溶液和硝酸 |
| D、硝酸钡溶液和盐酸 |
下列各组物质中的四种物质,用一种试剂即可鉴别的是( )
| A、甲酸、乙醛、甲酸钠溶液、乙酸乙酯 |
| B、丙烯、甲烷、乙炔、乙烯 |
| C、苯酚、乙醇、苯、四氯化碳 |
| D、苯乙烯、苯酚、乙苯、二甲苯 |
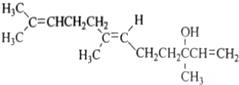
橙花醇具有玫瑰及苹果香气,可作为香料,其结构简式如图,下列关于橙花醇的叙述,错误的是( )

| A、分子式为C15H26O |
| B、既能发生取代反应,也能发生加成反应 |
| C、1mo1橙花醇在氧气中充分燃烧,需消耗470.4L氧气(标准状况) |
| D、1mo1橙花醇在室温下与溴四氯化碳溶液反应,最多消耗240g溴 |