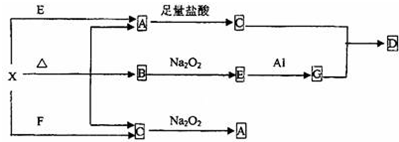
题目内容
下列化合物中,不能由单质之间直接化合生成的是( )
| A、Na2O |
| B、Na2O2 |
| C、CuCl2 |
| D、FeCl2 |
考点:钠的化学性质,氯气的化学性质
专题:
分析:金属单质与氯气反应得到最高价的金属氯化物,钠与氧气在常温下生成氧化钠,与氧气加热条件下生成过氧化钠.
解答:
解:A、钠与氧气在常温下生成氧化钠,故A不选;
B、钠与氧气加热条件下生成过氧化钠,故B不选;
C、Cu与氯气在点燃时能直接生成CuCl2,故C不选;
D、Fe和氯气在点燃时能直接生成FeCl3,故D选.
故选D.
B、钠与氧气加热条件下生成过氧化钠,故B不选;
C、Cu与氯气在点燃时能直接生成CuCl2,故C不选;
D、Fe和氯气在点燃时能直接生成FeCl3,故D选.
故选D.
点评:本题考查氯气的性质及其钠在不同条件下的产物,明确氯气具有强氧化性,与变价金属反应生成最高价金属氯化物是解答本题的关键,较简单.

练习册系列答案
相关题目
下列各组离子在指定溶液中一定能大量共存的是( )
| A、无色溶液中:K+、Cu2+、Na+、SO42- |
| B、强酸性溶液中:Al3+、NO3-、I-、Cl- |
| C、pH=11的溶液中:Na+、CO32-、AlO2-、NO3- |
| D、加入Al能放出H2的溶液中:NH4+、Cl-、HCO3-、NO3- |
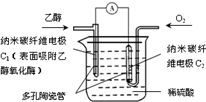 生物燃料电池(BFC)是以有机物为燃料,直接或间接利用酶作为催化剂的一类特殊的燃料电池,其能量转化率高,是一种真正意义上的绿色电池,其工作原理如图所示.已知C1极的电极反应方程式为:C2H5OH+3H2O-12e-=2CO2+12H+.下列说法不正确的是( )
生物燃料电池(BFC)是以有机物为燃料,直接或间接利用酶作为催化剂的一类特殊的燃料电池,其能量转化率高,是一种真正意义上的绿色电池,其工作原理如图所示.已知C1极的电极反应方程式为:C2H5OH+3H2O-12e-=2CO2+12H+.下列说法不正确的是( )| A、C1极为电池负极,C2极为电池正极 |
| B、C2极的电极反应式为O2+4H++4e-=2H2O |
| C、该生物燃料电池的总反应方程式为C2H5OH+3O2=2CO2+3H2O |
| D、电子由C2极经外电路导线流向C1极 |
下列说法正确的是( )
| A、物质发生化学变化都伴随着能量的变化 |
| B、任何反应中的能量变化都表现为热量变化 |
| C、伴有能量变化的物质变化都是化学变化 |
| D、需要加热才能发生的反应一定是吸热反应 |
2.4gCu投入适量的浓硝酸充分反应后,铜粉完全溶解,收集到1.2L标准状态下的气体,如将此气体通过足量水,最后收集到标准状况下气体的体积为( )
| A、560mL |
| B、448mL |
| C、600mL |
| D、400mL |
下列排列顺序正确的是( )
| A、常温下水电离出的c(H+):pH=5的CH3COOH溶液>pH=5的盐酸 |
| B、微粒半径:Fe(OH)3胶粒>K+>C1->Na+ |
| C、等温等物质的量浓度溶液的pH:Na2CO3>苯酚钠>NaHCO3 |
| D、氢化物的沸点:H2Se>H2S>H2O |
下列物质的化学用语正确的是( )
①NH4H的电子式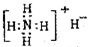
②硝基苯的结构简式:
③葡萄糖的实验式:CH2O
④甲烷分子的比例模型: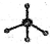
⑤Fe2+的离子结构:
⑥原子核内有10个中子的氧原子:
O.
①NH4H的电子式
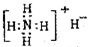
②硝基苯的结构简式:

③葡萄糖的实验式:CH2O
④甲烷分子的比例模型:

⑤Fe2+的离子结构:

⑥原子核内有10个中子的氧原子:
18 8 |
| A、②③⑥ | B、①③⑤⑥ |
| C、③⑥ | D、①②③④⑤⑥ |