题目内容
实验室常用Na2O2与H2O反应快速制取少量O2。用下面装置来制取O2并演示Na在O2中的燃烧实验。

请回答下列问题:
(1)关闭装置中的止水夹a后,开启活塞b,漏斗中液体不断地往下滴,直至全部流入试管。试判断装置是否漏气 (填“漏气”“不漏气”或“无法确定”),判断理由是 。
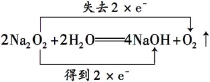
(2)写出A装置中反应的化学方程式并标出电子得失情况:
。
(3)C装置中观察到的现象是 。
(4)D装置中盛放的试剂是 ,其作用是
。
(1)漏气 漏斗中的液体能全部流入试管说明试管中压强与外界相同
(2)
(3)剧烈燃烧,发出黄光,有淡黄色物质生成
(4)碱石灰 防止空气中的H2O、CO2进入C装置
【解析】
试题分析:(1)关闭装置中的止水夹a后,开启活塞b,漏斗中液体不断地往下滴,直至全部流入试管,说明装置漏气,因为漏斗中的液体能全部流入试管,说明试管中压强与外界相同;
(2)A装置中反应是过氧化钠和水的反应,反应的化学方程式为2Na2O2+2H2O====4NaOH+O2↑反应的电子转移情况用双线桥标出电子得失情况为:
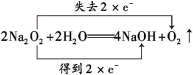 ;
;
(3)C装置中观察到的现象是钠在氧气中燃烧的实验现象,钠剧烈燃烧,发出黄光,有淡黄色物质生成;(4)为避免空气中的二氧化碳和水蒸气进入C装置与钠反应,影响实验现象的判断,干燥管中应装碱石灰。
考点:金属钠的性质与应用

练习册系列答案
相关题目


