题目内容
11.下列离子方程式中,书写不正确的是( )| A. | 用小苏打治疗胃酸过多:HCO3-+H+═CO2↑+H2O | |
| B. | 纯碱溶液与石灰水反应:Ca2++CO32-=CaCO3↓ | |
| C. | 铜粉与硝酸银溶液反应:Ag++Cu═Ag+Cu2+ | |
| D. | 盐酸滴在石灰石上:CaCO3+2H+=Ca2++CO2↑+H2O |
分析 A.小苏打为碳酸氢钠,碳酸氢钠与盐酸反应生成氯化钠、二氧化碳气体和水;
B.纯碱为碳酸钠,碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠;
C.离子方程式两边正电荷不相等,违反了电荷守恒;
D.石灰石的主要成分为碳酸钙,碳酸钙与盐酸反应生成氯化钙、二氧化碳气体和水.
解答 解:A.用小苏打治疗胃酸过多,胃酸中含有盐酸,该反应的离子方程式为:HCO3-+H+═CO2↑+H2O,故A正确;
B.纯碱溶液与石灰水反应的离子方程式为:Ca2++CO32-=CaCO3↓,故B正确;
C.铜粉与硝酸银溶液反应生成硝酸铜和银,正确的离子方程式为:2Ag++Cu═2Ag+Cu2+,故C错误;
D.盐酸滴在石灰石上,反应的离子方程式为:CaCO3+2H+=Ca2++CO2↑+H2O,故D正确;
故选C.
点评 本题考查了离子方程式的书写判断,为高考的高频题,题目难度不大,注意掌握离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)等.

练习册系列答案
相关题目
1.下列对某溶液所含离子检验的叙述正确的是( )
| A. | 滴入NaOH溶液,产生白色沉淀,则原溶液一定含有Mg2+ | |
| B. | 滴入BaCl2溶液和稀硝酸,产生白色沉淀,则原溶液一定含有SO42- | |
| C. | 滴入稀硫酸产生无色无味使澄清石灰水浑浊的气体,则原溶液一定含有CO32- | |
| D. | 滴入KSCN溶液呈无色,再通入少量Cl2后呈红色,则原溶液一定含有Fe2+ |
2.对 N2+3H2?2NH3 反应,仅改变下列一个条件,就能提高活化分子的浓度从而加快正反应速率的是 ( )
| A. | 加热 | B. | 增大体积 | C. | 加负催化剂 | D. | 补充 He |
19.用NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 0.5mol Mg与足量盐酸反应生成氢气的体积为11.2升 | |
| B. | 标准状况下,11.2L SO2所含的原子数为1.5NA | |
| C. | 8gCH4所含的氢原子数为0.5NA | |
| D. | 46g NO2和N2O4的混合物所含的分子数为1NA |
6.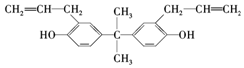 双酚A也称BPA(结构如图所示),严重威胁着胎儿和儿童的健康,甚至癌症和新陈代谢紊乱导致的肥胖也被认为与此有关.下列关于双酚A的说法正确的是( )
双酚A也称BPA(结构如图所示),严重威胁着胎儿和儿童的健康,甚至癌症和新陈代谢紊乱导致的肥胖也被认为与此有关.下列关于双酚A的说法正确的是( )
 双酚A也称BPA(结构如图所示),严重威胁着胎儿和儿童的健康,甚至癌症和新陈代谢紊乱导致的肥胖也被认为与此有关.下列关于双酚A的说法正确的是( )
双酚A也称BPA(结构如图所示),严重威胁着胎儿和儿童的健康,甚至癌症和新陈代谢紊乱导致的肥胖也被认为与此有关.下列关于双酚A的说法正确的是( )| A. | 该化合物的化学式为C20H22O2 | |
| B. | 该化合物能与三氯化铁溶液发生显色反应 | |
| C. | 该化合物的所有碳原子处于同一平面 | |
| D. | 1 mol双酚A最多可与4 mol Br2(溴水)发生取代反应 |
3.1,4-二氧六环是一种常见的溶剂,它可以通过下列方法合成,则烃A为( )
A烃类$\stackrel{Br_{2}}{→}$B$\stackrel{NaOH水溶液}{→}$C$→_{-H_{2}O}^{浓H_{2}SO_{4}}$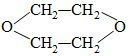
A烃类$\stackrel{Br_{2}}{→}$B$\stackrel{NaOH水溶液}{→}$C$→_{-H_{2}O}^{浓H_{2}SO_{4}}$
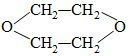
| A. | 乙烯 | B. | 1-丁稀 | C. | 1,3-丁二烯 | D. | 乙炔 |
20.下列离子方程式书写正确的是( )
| A. | 铁和稀盐酸的反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 铁与氯化铜溶液的反应:2Fe+3Cu2+═2Fe3++3Cu | |
| C. | 醋酸与NaOH溶液的反应:H++OH-═H2O | |
| D. | 碳酸镁与稀硫酸的反应:MgCO3+2H+═Mg2++H2O+CO2↑ |
1.在强酸性溶液中,下列离子组能大量共存且溶液为无色透明的是( )
| A. | Na+、K+、OH-、Cl- | B. | Cu2+、Cl-、SO42-、NO3- | ||
| C. | Mg2+、Na+、SO42-、Cl- | D. | Ca2+、HCO3-、NO3-、K+ |