题目内容
已知:①lmolH2分子中化学键断裂时需要吸收436kJ的能量②1mol C12分子中化学键断裂时需要吸收243kJ的能量③由H原子和C1原子形成l mol HCl分子时释放431kJ的能量下列叙述中正确的是( )
| A、氢气和氯气反应生成氯化氢气体的热化学方程式是:H2(g)+Cl2(g)=2HCl(g)△H=366KJ?mol-1 |
| B、氢气和氯气反应生成2 mol氯化氢气体,反应的△H=366KJ?mol-1 |
| C、氢气和氯气反应生成2mol氯化氢气体,反应的△H=-183KJ?mol-1 |
| D、氢气和氯气反应生成1 mol氯化氢气气体,反应的△H=-183KJ?mol-1 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:反应热等于反应物的总键能-生成物的总键,热化学方程式应标出反应热、各物质的状态,反应中的热量与反应物的物质的量成正比,据此分析.
解答:
解:H2(g)+Cl2(g)=2HCl(g)的反应热=生成物的键能减反应物的键能=436kJ?mol-1+243kJ?mol-1-2×431 kJ?mol-1=-183kJ?mol-1,故1mol氢气与1mol氯气反应生成2molHCl时放出热量为183KJ,△H=-183kJ/mol,
故选C.
故选C.
点评:本题主要考查了反应热的计算,难度不大,注意掌握热化学方程式的书写,明确反应热等于反应物的总键能-生成物的总键是关键.

练习册系列答案
相关题目
下列说法不正确的是( )
| A、Ksp只与难溶电解质的性质和温度有关 |
| B、由于Ksp(ZnS)>Ksp(CuS),所以ZnS沉淀在一定条件下可转化为CuS沉淀 |
| C、任意两种难溶电解质作比较时,Ksp小的,溶解度一定小 |
| D、t℃时,Ksp(CaCO3)=4×10-16,则CaCO3饱和溶液中c(Ca2+)=2×10-8 mol/L |
下列说法不正确的是( )
| A、浓硫酸能与铜反应释放出氢气 |
| B、浓硫酸能与灼热的木炭反应,生成二氧化碳和二氧化硫 |
| C、浓硫酸具有吸水性,在实验中常用作干燥剂 |
| D、冷的浓硫酸可以用铁质或铝质容器储存 |
下列三种化合物由左到右是按强电解质、弱电解质、非电解质的顺序排列的一组是( )
| A、HCl、CaCO3、SO2 |
| B、KNO3、CH3COOH、NH3 |
| C、HClO、H2S、C2H5OH |
| D、BaSO4、H3PO4、H2O |
下列各装置中都盛有0.1mol?L-1 的NaCl溶液,放置相同时间后,锌片的腐蚀速率由快到慢的顺序是( )
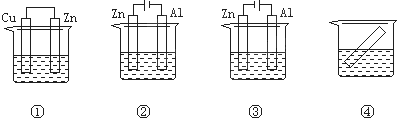

| A、③①④② | B、①②④③ |
| C、②①④③ | D、②①③④ |
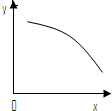 在一定条件下,固定容积的密闭容器中反应:2NO2(g)?O2(g)+2NO(g)△H>0,达到平衡.当改变其中一个条件x,y随x变化符合图中曲线的是( )
在一定条件下,固定容积的密闭容器中反应:2NO2(g)?O2(g)+2NO(g)△H>0,达到平衡.当改变其中一个条件x,y随x变化符合图中曲线的是( )| A、当x表示温度时,y表示NO物质的量 |
| B、当x表示反应时间时,y表示混合气体的密度 |
| C、当x表示压强时,y表示NO2的转化率 |
| D、当x表示NO2物质的量时,y表示O2的物质的量 |
改变下列某一条件:①浓度 ②压强 ③温度 ④催化剂,其中一定能使化学平衡发生移动的是( )
| A、①④ | B、②③ | C、①③ | D、②④ |
下列过程或事实不涉及氧化还原反应的是( )
①蔗糖炭化
②用氢氟酸雕刻玻璃
③铁遇冷的浓硫酸钝化
④装碱液的试剂瓶不用玻璃塞
⑤雷雨发庄稼
⑥浓硝酸常显黄色.
①蔗糖炭化
②用氢氟酸雕刻玻璃
③铁遇冷的浓硫酸钝化
④装碱液的试剂瓶不用玻璃塞
⑤雷雨发庄稼
⑥浓硝酸常显黄色.
| A、①③⑤⑥ | B、②④ |
| C、②④⑥ | D、①②③④⑤⑥ |