题目内容
在一定温度下,Na2CO3溶液中存在水解平衡:CO32-+H2O?HCO3-+OH-.下列说法中,正确的是( )A.升高温度,
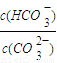 减小
减小B.加入NaOH固体,平衡向逆反应方向移动,溶液pH减小
C.稀释溶液,Na2CO3水解程度增大,水解平衡常数增大
D.氯化铵固体,平衡向正反应方向移动
【答案】分析:A、升高温度,促进碳酸根离子水解;
B、氢氧化钠中的氢氧根离子抑制了碳酸钠水解;
C、温度不变,水解平衡常数不变;
D、铵离子结合氢氧根离子,促进水解.
解答:解:A、温度升高,水解是吸热反应,平衡向着正反应方向移动,碳酸氢根物质的量增大,碳酸根离子物质的量减小,由于溶液体积不变,所以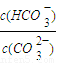 =
=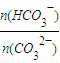 ,可见比值变大,故A错误;
,可见比值变大,故A错误;
B、氢氧化钠电离的氢氧根离子抑制了碳酸钠的水解,溶液中氢氧根离子浓度变大,溶液pH变大,故B错误;
C、稀释碳酸钠溶液后,促进了碳酸钠的水解,温度不变,水解平衡常数不变,故C错误;
D、加入氯化铵,铵离子结合溶液中的氢氧根离子,促进了水解,平衡向着正向移动,故D正确;
故选D.
点评:本题考查了影响盐类水解的因素,水解平衡常数只受温度影响,本题难度不大.
B、氢氧化钠中的氢氧根离子抑制了碳酸钠水解;
C、温度不变,水解平衡常数不变;
D、铵离子结合氢氧根离子,促进水解.
解答:解:A、温度升高,水解是吸热反应,平衡向着正反应方向移动,碳酸氢根物质的量增大,碳酸根离子物质的量减小,由于溶液体积不变,所以
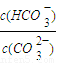 =
=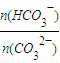 ,可见比值变大,故A错误;
,可见比值变大,故A错误;B、氢氧化钠电离的氢氧根离子抑制了碳酸钠的水解,溶液中氢氧根离子浓度变大,溶液pH变大,故B错误;
C、稀释碳酸钠溶液后,促进了碳酸钠的水解,温度不变,水解平衡常数不变,故C错误;
D、加入氯化铵,铵离子结合溶液中的氢氧根离子,促进了水解,平衡向着正向移动,故D正确;
故选D.
点评:本题考查了影响盐类水解的因素,水解平衡常数只受温度影响,本题难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
|
一定温度下,可逆反应A2(s)+3B2(g) | |
| [ ] | |
A. |
容器内每减少1 mol A2,同时消耗2 mol AB3 |
B. |
容器内nA2∶nB2∶nAB3=1∶3∶2 |
C. |
混合气体总的物质的量 |
D. |
容器内的气体密度不再改变 |
一定温度下,可逆反应A2(s)+3B2(g) 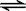 2AB3(g)在可变容器中不能作为达到平衡的标志是
2AB3(g)在可变容器中不能作为达到平衡的标志是
| A.容器内每减少1mol A2,同时消耗2mol AB3 |
| B.容器内nA2:nB2:nAB3=1:3:2 |
| C.混合气体总的物质的量 |
| D.容器内的气体密度不再改变 |
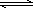 2AB3(g)在可变容器中不能作为达到平衡的标志是
2AB3(g)在可变容器中不能作为达到平衡的标志是 2AB3(g)在可变容器中不能作为达到平衡的标志是
2AB3(g)在可变容器中不能作为达到平衡的标志是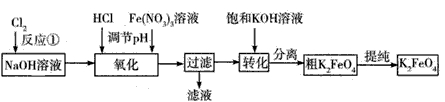
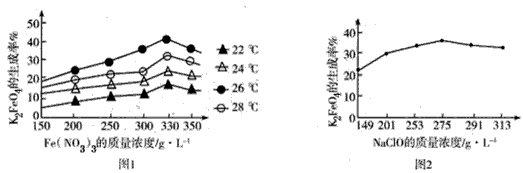
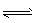 4Fe(OH)3+8OH-+3O2↑。在“提纯”K2FeO4的过程中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用__(填序号)。
4Fe(OH)3+8OH-+3O2↑。在“提纯”K2FeO4的过程中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用__(填序号)。