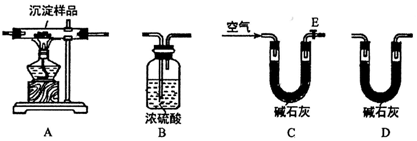
题目内容
6.下列变化过程中,共价键被破坏的是( )| A. | 冰融化成水 | B. | 氯气溶于水 | C. | 氯化钠熔化 | D. | 酒精溶于水 |
分析 首先判断晶体的类型,明确晶体中粒子间的作用力,根据物质的变化判断共价键是否被破坏.
解答 解:A、冰融化成水时破坏的是氢键和范德华力,故A错误;
B、氯气溶于水,生成氯化氢和次氯酸,破坏共价键和共价键的形成,故B正确;
C、氯化钠属于离子晶体,氯化钠熔化时破坏离子键,故C错误;
D、酒精溶于水,是氢键的形成,是物理变化,故D错误;
故选:B.
点评 本题考查化学键类型的判断,题目难度不大,注意晶体的类型,分子间作用力和化学键的区别.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.工业纯碱中常含有少量的NaCl杂质,某化学兴趣小组取m g纯碱样品与足量稀盐酸充分反应,加热、蒸干、灼烧,得ng固体.则该样品中纯碱的质量分数为( )
| A. | $\frac{106(m-n)}{11m}$×100% | B. | $\frac{168(m-n)}{56m}$×100% | C. | $\frac{84(n-m)?}{11m}$×100% | D. | $\frac{?(n-m)?}{m}$×100% |
17.汽车铅蓄电池总反应:Pb+PbO2+2H3SO4═2PbSO4↓+2H3O,有关说法不正确的是( )
| A. | Pb 为负极,发生还原反应 | |
| B. | 放电过程,正负极质量均增重 | |
| C. | 导线中每通过 1mole-,溶液中减少 2molH+ | |
| D. | 电子由 Pb 经外电路流向 PbO3 |
1.已知氢化锂固体不导电,隔绝空气熔融时能导电,它跟水反应能生成一种相同条件下密度最小的气体.下列有关氢化锂的说法中,不正确的是( )
| A. | 氢化锂是一种电解质 | B. | LiH是离子晶体[ | ||
| C. | LiH是一种强氧化剂 | D. | LiH中Li+半径小于H-半径 |
11.一定温度下用过量铁块与稀硫酸反应制取氢气,采取下列措施:
①将铁块换为等质量的铁粉;
②加入少量NaNO3固体;
③加入少量硫酸氢钠固体;
④延长反应时间;
⑤加热;
⑥将稀硫酸换成98%硫酸,
其中可增大单位时间内氢气收集量的措施有( )
①将铁块换为等质量的铁粉;
②加入少量NaNO3固体;
③加入少量硫酸氢钠固体;
④延长反应时间;
⑤加热;
⑥将稀硫酸换成98%硫酸,
其中可增大单位时间内氢气收集量的措施有( )
| A. | ①②④ | B. | ①③⑤ | C. | ②④⑤ | D. | ①⑤⑥ |
2.向60mLNa2SO4溶液中加入BaCl2溶液,有关数据见表( )
| 实验编号 | 1 | 2 | 3 | 4 | 5 |
| BaCl2溶液体积/mL | 0 | 30 | 60 | 100 | 120 |
| 沉淀质量/g | 0 | 0.699 | x | 2.097 | 2.097 |
| A.混合前,BaCl2溶液的物质的量浓度为0.10mol•L-1 |
| B.混合前,Na2SO4溶液的物质的量浓度为0.15mol•L-1 |
| C.3号实验中沉淀的质量x为1.398g |
| D.完全沉淀60mL Na2SO4溶液消耗BaCl2溶液的体积为80mL |
| A. | A | B. | B | C. | C | D. | D |
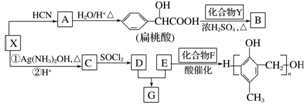
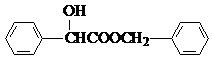 .
.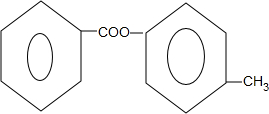 +2NaOH$\stackrel{△}{→}$
+2NaOH$\stackrel{△}{→}$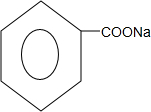 +
+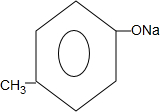 +H2O.
+H2O.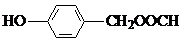 ,
,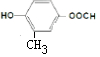 ,
, .
.