题目内容
(16分)水中氧的含量测定步骤如下:
步骤1:水中的氧在碱性溶液中将Mn2+氧化为MnO(OH)2。
步骤2:加入碘离子将生成的MnO(OH)2再还原成Mn2+离子。
步骤3:用硫代硫酸钠标准溶液滴定步骤2中生成的碘。
有关的测定数据如下:
1:Na2S2O3溶液的标定。取25.00 mL KIO3标准溶液(KIO3浓度:174.8 mg?L-1)与过量KI在酸性介质中反应,用Na2S2O3溶液滴定,消耗12.45 mL。
2:取20.0°C下新鲜水样103.5mL,按上述测定步骤滴定,消耗Na2S2O3标准溶液11.80 mL。已知该温度下水的饱和O2含量为9.08 mg?L-1。
3.在20.0°C下密闭放置5天的水样102.2 mL,按上述测定步骤滴定,消耗硫代硫酸钠标准溶液6.75 mL。
5-1 写出上面3步所涉及的化学反应方程式。
5-2 计算标准溶液的浓度(单位mol?L-1)。
5-3 计算新鲜水样中氧的含量(单位mg?L-1)。
5-4 计算陈放水样中氧的含量(单位mg?L-1)。
5-5 以上测定结果说明水样具有什么性质?
5-1 步骤1 2Mn2+ + O2 + 4OH = 2MnO(OH)2 (1分)
步骤2 2I + MnO(OH)2 + 4H+ = Mn2+ + I2 + 3H2O (1分)
或 ![]()
步骤3 I2 + 2S2O32 = 2I + S4O62 (1分)
或 ![]()
5-2 标准溶液的浓度:9.841´103 mol?L-1
计算过程:
c(IO3) = 174.8´103 g?L-1 / 214.0g?mol-1 = 8.168 ´ 104 mol?L-1 (1分)
c(S2O32)= 6´ c(IO3) ´V(IO3)/V(S2O32)
= 6´8.168´104mol?L-1´25.00mL/12.45mL=9.841´103mol?L-1 (3分)
5-3 新鲜水样中氧的含量: 8.98 mg?L-1
计算过程: 103.5mL水样中氧的含量:
n(O2) = 0.25´c(S2O32-)´V(S2O32-)
=0.25´9.841´10-3mol?L -1´11.80´10-3L=2.903´10-5 mol
氧含量: r(O2) = 2.903´10-5 mol´32.00´103mg?mol-1/103.5´10-3L
= 8.98mg?L-1 (3分)
注: 新鲜水样的氧饱和度= (8.98/9.08) ´100%= 98.9%
5-4 陈放水样中氧的含量: 5.20 mg?L-1
计算过程: 102.2mL中氧的含量:
n(O2) = 0.25´c(S2O32-)´V(S2O32-)
= 0.25´9.841´10-3mmol?mL-1´6.75 mL= 1.66´10-2 mmol
氧含量: r(O2) = 1.66´10-2 mmol´32.00mg?mmol-1/102.2´10-3L = 5.20 mg?L-1 (3分)
注: 陈放引起氧的消耗量= 8.98mg?L-1 5.20mg?L-1 = 3.78 mg?L-1
5-5 表明水样里存在好氧性(或喜氧性)微生物(1.5分)或者存在能被氧气还原
的还原性物质(1.5分)。 (共3分)
注:若计算结果正确,任何正确计算过程均得满分;若浓度值错误, 再看计算过程, 若关系式正确, 运算错误, 给一半分。w.w.w.k.s.5.u.c.o.m

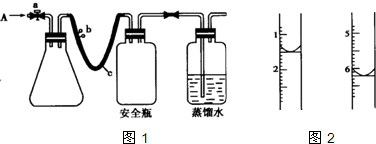
 硫酸工业尾气中二氧化硫含量超过0.05%(体积分数)时需经处理后才能排放.某校兴趣小组欲测定硫酸工业尾气中二氧化硫含量,采用以下方案:
硫酸工业尾气中二氧化硫含量超过0.05%(体积分数)时需经处理后才能排放.某校兴趣小组欲测定硫酸工业尾气中二氧化硫含量,采用以下方案: