题目内容
2.若某地每升海水中含钠元素11.5g,则该海水中氯化钠(设钠都以氯化钠的形式存在)的含量为( )| A. | 23g/L | B. | 27.2g/L | C. | 29.25g/L | D. | 32.4g/L |
分析 根据氯化钠的化学式NaCl计算出每升海水中含含有氯化钠的质量,从而可知该海水中氯化钠(设钠都以氯化钠的形式存在)的含量,据此进行解答.
解答 解:每升海水中含钠元素11.5g,则每升海水中含NaCl的质量为:11.5g×$\frac{58.5}{23}$=29.25g,
所以该海水中氯化钠(设钠都以氯化钠的形式存在)的含量为29.25g/L,
故选C.
点评 本题考查了物质的量的计算,题目难度不大,正确分析海水中钠元素与氯化钠之间的关系为解答关键,试题侧重考查学生的分析能力及化学计算能力.

练习册系列答案
相关题目
12.在一定量的密闭容器中进行反应:N2(g)+3H2(g)?2NH3(g).已知反应过程中某一时刻N2、H2、NH3的浓度分别为0.1mol/L、0.3mol/L、0.2mol/L.当反应达到平衡时,可能存在的数据是( )
| A. | N2、H2均为0.18mol/L | B. | N2为0.15mol/L | ||
| C. | N2为0.2mol/L,H2为0.6mol/L | D. | NH3为0.4mol/L |
17.有关能量的判断或表示方法正确的是( )
| A. | 反应A(g)+B(g)═2C(s)可以自发进行,则其必为放热反应 | |
| B. | 从C(石墨,s)═C(金刚石,s)△H=+1.9 kJ/mol,可知:金刚石比石墨更稳定 | |
| C. | 等质量的硫蒸气和硫固体分别完全燃烧,后者放出热量更多 | |
| D. | 若2H2(g)+O2(g)=2H2O(g)△H=-483.6 kJ•mol-1,则H2燃烧热为241.8 kJ•mol-1 |
2.1mol乙烯和氯气发生加成反应生成氯乙烷,该氯乙烷继续和Cl2发生取代反应,最多可再消耗Cl2的物质的量为( )
| A. | 4mol | B. | 3mol | C. | 5mol | D. | 2.5mol |
3.铁有δ、γ、α三种同素异形体,如下图所示,三种晶体在不同温度下能发生转化.下列说法不正确的是( )
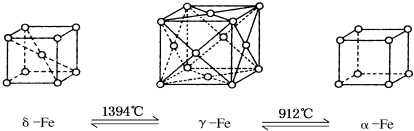

| A. | 将铁加热到1500°C分别急速冷却和缓慢冷却,得到的晶体类型相同 | |
| B. | α-Fe晶体中与每个铁原子等距离且最近的铁原子有6个 | |
| C. | 若δ-Fe晶胞边长为a cm,α-Fe晶胞边长为b cm,则两种晶体密度比为2b3:a3 | |
| D. | δ-Fe晶体中与每个铁原子等距离且最近的铁原子有8个 |
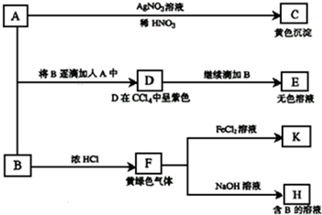
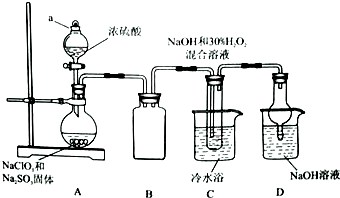 实验室欲制备高效漂白剂亚氯酸钠(NaCLO2),并对其样品进行分析.
实验室欲制备高效漂白剂亚氯酸钠(NaCLO2),并对其样品进行分析.