题目内容
下列说法正确的是( )
| A、难溶电解质的溶度积越小,溶解度越大 |
| B、一定浓度的NH4Cl溶液可以溶解Mg(OH)2 |
| C、升高温度,物质的溶解度都会增大 |
| D、可以通过沉淀反应使杂质离子完全沉淀 |
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:A、溶度积比较难溶物质溶解度,需要阴阳离子比相同条件下,才可以进行比较;
B、依据平衡Mg(OH)2(固)?Mg2++2OH-,和反应NH4++OH-?NH3?H2O方向判断;
C、升温物质的溶解度可能是增大,也可能是减小;
D、沉淀反应是平衡状态不能完全沉淀;
B、依据平衡Mg(OH)2(固)?Mg2++2OH-,和反应NH4++OH-?NH3?H2O方向判断;
C、升温物质的溶解度可能是增大,也可能是减小;
D、沉淀反应是平衡状态不能完全沉淀;
解答:
解:A、阴阳离子比相同条件下,可以用溶度积常数大小进行比较,难溶电解质的溶度积越小,溶解度越小,阴阳离子比不同的不能用溶度积常数直接进行比较,故A错误;
B、由于NH4Cl电离出的NH4+与Mg(OH)2电离出的OH-结合,生成了弱的电解质NH3?H2O,导致沉淀溶解的平衡右移,Mg(OH)2沉淀溶解,故B正确;
C、升温物质的溶解度可能是增大,也可能是减小,如硝酸钾溶解度谁温度升高增大,氢氧化钙溶解度随温度升高减小,故C错误;
D、沉淀反应是一定条件下的平衡状态,是可逆过程,不能进行彻底,通过沉淀反应不能使杂质离子完全沉淀,故D错误;
故选B.
B、由于NH4Cl电离出的NH4+与Mg(OH)2电离出的OH-结合,生成了弱的电解质NH3?H2O,导致沉淀溶解的平衡右移,Mg(OH)2沉淀溶解,故B正确;
C、升温物质的溶解度可能是增大,也可能是减小,如硝酸钾溶解度谁温度升高增大,氢氧化钙溶解度随温度升高减小,故C错误;
D、沉淀反应是一定条件下的平衡状态,是可逆过程,不能进行彻底,通过沉淀反应不能使杂质离子完全沉淀,故D错误;
故选B.
点评:本题考查了难溶物的沉淀溶解平衡状态发信息判断,溶解度大小比较的依据是解题关键,题目难度中等.

练习册系列答案
相关题目
“绿色化学”提倡化工生产应尽可能将反应物的原子全部利用,从根本上解决环境污染问题.在下列制备环氧乙烷的反应中,最符合“绿色化学”思想的是( )
A、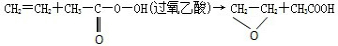 |
| B、CH2=CH2+Cl2+Ca(OH)2→CH2-CH2+CaCl2+H2O |
C、 |
D、 |
向一强酸HA溶液中加入一碱MOH,反应后溶液呈中性,下列判断正确的是( )
| A、加入的碱过量 |
| B、生成的盐不水解 |
| C、酸与碱等物质的量混合 |
| D、反应后溶液中c(A-)=c(M+) |
下列有关离子方程式书写错误的是( )
| A、将标准状况下1.12L氯气通入10mL 1mol/L的溴化亚铁溶液中:2Fe2++4Br-+3Cl2=2Fe3++6Cl-+2Br2 |
| B、向NaOH溶液中滴加同浓度的少量Ca(HCO3)2溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O |
| C、向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至刚好沉淀完全:Ba2++2OH-+H++SO42-+NH4+=BaSO4↓+NH3?H2O+H2O |
| D、向NaHSO3溶液中滴入适量NaClO溶液:HSO3-+ClO-=SO42-+H++Cl- |
下列物质中,属于电解质的是( )
| A、铜丝 |
| B、MgCl2 |
| C、CO2 |
| D、蔗糖 |
碘化钠与浓硫酸反应,反应方程式如下所示:8NaI+9H2SO4→8NaHSO4+4I2+H2S+4H2O;上述反应中哪种离子被氧化( )
| A、H+ |
| B、I- |
| C、Na+ |
| D、SO42- |
C6H14的各种同分异构体中,整个分子所含甲基数和它的一氯取代物的数目下列相符的是( )
| A、2个甲基,可能生成4种一氯代物 |
| B、3个甲基,可能生成5种一氯代物 |
| C、3个甲基,可能生成3种一氯代物 |
| D、4个甲基,可能生成4种一氯代物 |
 电解原理在化学工业中有广泛应用.如表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: