题目内容
下列各组物质中,所含分子数不相同的是( )
| A、2.24L H2(标准状况)和0.1mol N2 |
| B、5.6L N2(标准状况)和11g CO2 |
| C、10g H2和10g O2 |
| D、9g H2O和0.5mol Br2 |
考点:物质的量的相关计算
专题:阿伏加德罗常数和阿伏加德罗定律
分析:各物质的物质的量相等,则含有分子数目相等,根据n=
=
计算判断.
| m |
| M |
| V |
| Vm |
解答:
解:A.标况下2.24L 氢气的物质的量为0.1 mol,与0.1mol氮气含有分子数目相等,故A不选;
B.标况下5.6L 氮气的物质的量=
=0.25mol,11g二氧化碳的物质的量=
=0.25mol,二者物质的量相等,故含有分子数目相等,故B正确;
C.氢气和氧气的摩尔质量本题,所以等质量的氢气和氧气的物质的量不相等,含有的分子数目也不相等,故C选,
D.9g水的物质的量为0.5mol,与0.5molBr2含有分子数目相等,故D不选,
故选C.
B.标况下5.6L 氮气的物质的量=
| 5.6L |
| 22.4L/mol |
| 11g |
| 44g/mol |
C.氢气和氧气的摩尔质量本题,所以等质量的氢气和氧气的物质的量不相等,含有的分子数目也不相等,故C选,
D.9g水的物质的量为0.5mol,与0.5molBr2含有分子数目相等,故D不选,
故选C.
点评:本题考查物质的量有关计算,比较基础,注意对公式的理解与灵活应用.

练习册系列答案
 应用题作业本系列答案
应用题作业本系列答案
相关题目
 在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系.下列条件下关于离子存在的说法中正确的是( )
在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系.下列条件下关于离子存在的说法中正确的是( )| A、a点对应的溶液中大量存在:Na+、Ba2+、Fe3+、Cl- |
| B、b点对应的溶液中大量存在:NH4+、K+、I-、NO3- |
| C、c点对应的溶液中大量存在:Cu2+、Na+、Cl-、S2- |
| D、d点对应的溶液中大量存在:K+、AlO2-、ClO-、Cl- |
关于下列各图的叙述正确的是( )
A、 表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为483.6kJ?mol-1 |
B、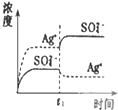 表示向Ag2SO4饱和溶液中加入等体积Na2SO4稀溶液,平衡会向左移动,Ksp减小 |
C、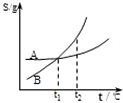 表示A、B两物质的溶解度随温度变化情况,将A、B饱和溶液分别由t1℃升温至t2℃时,溶质的质量分数B>A |
D、 表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同浓度的NaA溶液的pH小于NaB溶液 |
下列反应中Fe3+离子表现氧化性的是( )
| A、FeCl3溶液滴入沸水中,溶液变为红褐色 |
| B、FeCl3溶液中加入NaOH溶液产生红褐色沉淀 |
| C、FeCl3溶液中加入AgNO3溶液产生白色沉淀 |
| D、FeCl3溶液中通入H2S气体产生浅黄色S沉淀 |
下列说法中正确的是( )
| A、除去乙烷中混有的乙烯的方法是通氢气在一定条件下反应,使乙烯转化为乙烷 |
| B、苯、溴苯在常温、常压下为无色且密度比水小的液体 |
| C、丙烯与2-丁烯都存在順反异构体 |
| D、苯不能与溴水发生加成反应,也不能被酸性KMnO4溶液氧化 |
已知两种弱酸HA、HB的电离平衡常数Ka(HA)>Ka(HB).下列有关说法正确的是( )
| A、等温浓度均为0.1mol?L-1的HA、HB溶液中,其溶液的pH大小为:pH(HA)>pH(HB) |
| B、在0.1mol?L-1的NaA溶液中各离子浓度关系为:c(Na+)>c(A-)>c(OH-)>c(H+) |
| C、等体积pH相同的HA、HB溶液,分别加入等浓度的NaOH溶液,恰好完全反应消耗的NaOH溶液体积HA比HB多 |
| D、等温浓度均为0.1mol?L-1的NaA、NaB溶液中,其溶液的pH大小为:pH(NaA)>pH(NaB) |
分类是学习化学的重要方法,下列归纳正确的是( )
| A、纯碱、烧碱都属于碱类 |
| B、冰和干冰既是纯净物又是化合物 |
| C、铅笔芯、铅球主要成分都是铅 |
| D、液氯和氯水是同一种物质 |
下列各种冶炼方法中,可制得相应的金属的是( )
| A、电解熔融氯化铝制铝 |
| B、加热氧化银制银 |
| C、电解氯化钠溶液制钠 |
| D、氯化钠与铝粉高温共热制钠 |