题目内容
有A、B两种常温下有刺激性气味的气体,将黄绿色气体A通入品红溶液中,品红溶液变为无色;将气体B通入品红溶液中,品红溶液也变为无色;将气体A和气体B按1∶1的体积比混合充分,通入品红溶液中,品红溶液不褪色,通入紫色石蕊试液中,溶液只变红不褪色。试回答下列问题:
(1)写出A、B的化学式: 、 。
(2)写出A和NaOH溶液反应的化学方程式:
。
(3)写出B与NaOH溶液反应的离子方程式:
。
(4)写出A与B按1∶1的体积比混合通入水中充分反应的化学方程式:
。
(5)加热通入A后变为无色的品红溶液,现象是
;
加热通入B后变为无色的品红溶液,现象是
。
(1)Cl2 SO2 (2)Cl2+2NaOH====NaCl+NaClO+H2O
(3)SO2+2OH-====S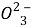 +H2O (4)Cl2+SO2+2H2O====H2SO4+2HCl
+H2O (4)Cl2+SO2+2H2O====H2SO4+2HCl
(5)无明显现象 溶液变红
【解析】
试题分析:(1)具有漂白作用,能使品红溶液褪色的气体有Cl2、SO2等,黄绿色气体A通入品红溶液中,品红溶液变为无色,所以A为Cl2,将气体B通入品红溶液中,品红溶液也变为无色,则B为SO2;(2)氯气在NaOH溶液中自身发生氧化还原反应生成NaCl和NaClO,反应的方程式为Cl2+2NaOH====NaCl+NaClO+H2O;(3)二氧化硫为酸性气体,与NaOH反应生成Na2SO3,反应的离子方程式为SO2+2OH-====S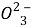 +H2O;(4)Cl2与SO2发生氧化还原反应生成H2SO4和HCl,反应的化学方程式为Cl2+SO2+2H2O====H2SO4+2HCl;(5)二氧化硫具有漂白性,漂白原理是与有色物质发生化合反应生成不稳定的无色物质,不稳定,加热后能够复原,而氯气的漂白原理是由于氯气和水反应生成具有强氧化性的次氯酸,不能复原。
+H2O;(4)Cl2与SO2发生氧化还原反应生成H2SO4和HCl,反应的化学方程式为Cl2+SO2+2H2O====H2SO4+2HCl;(5)二氧化硫具有漂白性,漂白原理是与有色物质发生化合反应生成不稳定的无色物质,不稳定,加热后能够复原,而氯气的漂白原理是由于氯气和水反应生成具有强氧化性的次氯酸,不能复原。
考点:二氧化硫的性质和作用

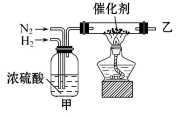
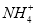 中,NH3发生氧化反应
中,NH3发生氧化反应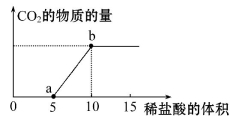
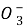 的物质的量浓度之比为2∶1,则滴入的稀盐酸中的HCl的物质的量等于 mol(用含字母m的代数式表示)。
的物质的量浓度之比为2∶1,则滴入的稀盐酸中的HCl的物质的量等于 mol(用含字母m的代数式表示)。