题目内容
2. 某校高三同学高考前重做以下两个课本实验,请你回答实验过程中的相关问题:
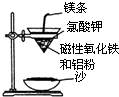
某校高三同学高考前重做以下两个课本实验,请你回答实验过程中的相关问题:(1)铝热反应实验:取磁性氧化铁粉按课本中的实验装置(如图)进行铝热反应,将反应后所得“铁块”溶于盐酸,向反应后的溶液中滴加KSCN溶液,发现溶液变血红色.
①出现这种现象的原因,除了因“铁块”中可能混有没反应完的磁性氧化铁外,还有一种可能原因是熔融的铁被空气中氧气氧化.
②若要证明反应所得“铁块”中含有金属铝,可用NaOH(填化学式)溶液,所发生反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑.
(2)化学反应速率影响因素的探究实验:
KI在经酸化的溶液中被空气氧化的反应式为:4H++4I-+O2=2I2+2H2O.该反应的速率受温度、酸度、溶剂、试剂浓度等影响,可用淀粉与碘的显色反应来观测该反应的速率.已知,淀粉与碘的显色反应在温度升高时灵敏度会降低,高于75℃则不能显色;淀粉浓度越高显色越灵敏、颜色也越深.
实验小组拟用0.8mol•L-1 KI溶液、0.1mol•L-1H2SO4溶液、淀粉溶液等来探究温度、酸度对上述反应速率的影响,他们做了A-C三组实验,部分实验数据如下表:
| 编号 | 温度/℃ | H2SO4体积/mL | KI溶液体积/mL | H2O体积/mL | 淀粉溶液 /mL | 出现蓝色时间/s |
| A | 39 | 10 | 5 | 5 | 1 | 5 |
| B | TB | 10 | 5 | 5 | 1 | 没出现蓝色 |
| C | 5 | 10 | 5 | 5 | 1 | 39 |
| D | t |
②A-C三组实验时,都加入了5mL水,其目的是为了在后续研究酸度因素对反应速率影响时保持KI和淀粉浓度不变(凡表达出“控制变量”、“对比实验”意思的各种合理答案都得分).
③B组实验中“没出现蓝色”,原因是温度(TB)高于75℃,淀粉与碘不显色.
④请你为小组设计D组实验方案(在表格空白处填入你设计的5个数据),以帮助小组完成探究目标.
⑤按你设计的实验数据,请你预测一个t值,并写出与你预测相对应的探究实验结论.
分析 (1)①考虑生成的熔融的铁的还原性,可以被空气中的氧气氧化导致生成三价的铁;
②根据铝与铁的性质的差异性来选择试剂,并写出反应的化学方程式;
(2)①确保A组实验在39℃下进行,可以采用水浴加热的方法;
②探究化学反应速率的影响因素时,需要保证变量的唯一性;
③根据“淀粉与碘的显色反应在温度升高时灵敏度会降低,高于75℃则不能显色”进行判断;
④根据ABC探究的是温度对反应速率的影响可知,D应该为探究酸度对反应速率的影响,据此完成本题;
⑤酸溶液浓度越大,反应速率越快,需要的时间越少,据此设计实验并写出结论.
解答 解:(1)①铝热反应生成的熔融的铁具有很强的还原性,可以被空气中的氧气氧化导致生成三价的铁,
故答案为:熔融的铁被空气中氧气氧化;
②要证明“铁块”中含有金属铝,应利用铁和铝性质的差异性,即铁不能和碱反应,而铝可以,故应选择氢氧化钠溶液,与铝反应的离子方程式为:
2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案为:NaOH;2Al+2OH-+2H2O=2AlO2-+3H2↑;
(2)①为确保A组实验在39℃下进行,应采用的控温操作方法为:将量出的各种溶液分别装在试管中,再将试管全部放在同一水浴中加热,用温度计测量试管中溶液的温度,
故答案为:将量出的各种溶液分别装在试管中,再将试管全部放在同一水浴中加热,用温度计测量试管中溶液的温度;
②为了在后续研究酸度因素对反应速率影响时保持KI和淀粉浓度不变,所以在A-C三组实验时,都加入了5mL水,
故答案为:为了在后续研究酸度因素对反应速率影响时保持KI和淀粉浓度不变(凡表达出“控制变量”、“对比实验”意思的各种合理答案都得分);
③淀粉与碘的显色反应在温度升高时灵敏度会降低,高于75℃则不能显色,所以B组实验中“没出现蓝色”,可能是温度(TB)高于75℃,淀粉与碘不显色,
故答案为:温度(TB)高于75℃,淀粉与碘不显色;
④A-C三组实验探究了温度对反应速率的影响,实验的目的是探究温度和酸度对反应速率的影响,则D的目的是探究酸度对反应速率的影响,所以温度可以为39或5℃,硫酸体积可以为15mL,水、碘化钾溶液的体积为5mL,淀粉溶液为1mL,
故答案为:
| D | 39或5 | 15 | 5 | 5 | 1 |
⑤当酸溶液体积小于10mL时,反应速率减小,当水溶液体积减小时,反应速率加快,即:酸体积<10mL时,t预测值要小于同温对比值;若酸体积>10mL时,t预测值要大于同温对比值,据此可以得出结论为:酸度越大反应速率越快,
故答案为:设计酸体积<10mL时,t预测值要小于同温对比值;设计酸体积>10mL时,t预测值要大于同温对比值;酸度越大反应速率越快.
点评 本题考查铝热反应、探究影响化学反应速率因素等知识点,为高频考点,明确影响化学反应速率原理、铝热反应原理是解本题关键,注意:探究影响化学反应速率因素时必须只有一个因素不同,其它因素必须完全相同,题目难度中等.

| A. | 开始析出晶体后用玻璃棒搅拌 | |
| B. | 滤去不溶性杂质后,将滤液移至坩埚内加热浓缩 | |
| C. | 当蒸发到剩余少量液体时,停止加热,利用余热将液体蒸干 | |
| D. | 将制得晶体转移到新制过滤器中用大量水进行洗涤 |
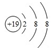
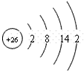
| A. | 过氧化钠的电子式: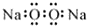 | B. | Cl-离子的结构示意图: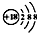 | ||
| C. | 二氧化硅的分子式:SiO2 | D. | HClO的结构式为H-O-Cl |
| A. | 工厂中常用的静电除尘装置是根据胶体粒子的带电性而设计的 | |
| B. | 过氧化钠(Na2O2)常用于呼吸面具或潜水艇中作为氧气的来源 | |
| C. | 波尔多液(CuSO4)常用来配制农药,主要因为Cu2+具有氧化性 | |
| D. | 明矾[KAl(SO4)2•12H2O]常用于自来水的净化,主要是因为胶体的吸附性 |
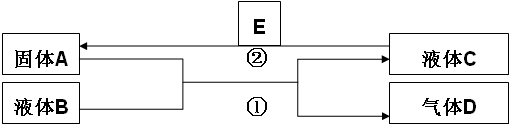
查阅资料得到以下有关高氯酸的信息:
| 名称 | 分子式 | 外观 | 沸点 |
| 高氯酸 | HClO4 | 无色液体 | 130℃ |

(1)操作①的名称是过滤.
(2)反应器Ⅰ中投料时需加入过量浓硫酸,请简述目的为了产物能得到HClO4而不是NaClO4.
(3)反应器Ⅱ中发生反应的离子方程式为4OH-+SO2+2ClO2=2ClO2-+SO42-+2H2O.
(4)某学习小组模拟工业流程图中的蒸馏过程,有液体流出时立即收集产品以获得HClO4纯品.请评价这一操作是否合理并说明理由不合理,因为水的沸点是100℃,HClO4的沸点是130℃,所以最先蒸馏流出的是水而不是HClO4.
(5)若想得到201kg的 HClO4纯品,至少需要NaClO3639kg.
(6)工业上也可用铂作阳极、铜作阴极电解盐酸制得高氯酸,在阳极区可得到20%的高氯酸.写出阳极的电极反应式(其中盐酸与高氯酸以化学式出现)4H2O+HCl-8e-=HClO4+8H+.
| A. | 1-氯丙烯 | B. | 丙烯 | C. | 2-甲基-2-丁烯 | D. | 1-丁烯 |
 .
.
 .
.