题目内容
13.下列离子方程式书写正确的是( )| A. | 钠与水反应:Na+H2O═Na++OH-+O2↑ | |
| B. | 氯化铁溶液和氢氧化钠溶液反应:Fe3++3OH-═Fe(OH)3↓ | |
| C. | 氯化铝溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ | |
| D. | 碳酸钙与稀盐酸反应:CO32-+2H+═CO2↑+H2O |
分析 A.电子、电荷不守恒,生成NaOH和氢气;
B.反应生成氢氧化铁和氯化钠;
C.反应生成氢氧化铝和氯化铵;
D.碳酸钙在离子反应中保留化学式.
解答 解:A.钠与水反应的离子反应为2Na+2H2O═2Na++2OH-+H2↑,故A错误;
B.氯化铁溶液和氢氧化钠溶液反应的离子反应为Fe3++3OH-═Fe(OH)3↓,故B正确;
C.氯化铝溶液中加入足量的氨水的离子反应为Al3++3NH3.H2O═Al(OH)3↓+3NH4+,故C错误;
D.碳酸钙与稀盐酸反应的离子反应为CaCO3+2H+═Ca2++CO2↑+H2O,故D错误;
故选B.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、氧化还原反应的离子反应考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4.下列说法中不正确的是( )
①由同一种元素组成的物质一定是单质
②阴离子一定不含金属元素,阳离子一定含金属元素
③碱性氧化物一定是金属氧化物
④酸性氧化物一定是非金属氧化物
⑤按酸分子中电离出的氢离子数目不同,可将酸分为一元酸、二元酸和多元酸
⑥无氧酸一定是非金属的氢化物.
①由同一种元素组成的物质一定是单质
②阴离子一定不含金属元素,阳离子一定含金属元素
③碱性氧化物一定是金属氧化物
④酸性氧化物一定是非金属氧化物
⑤按酸分子中电离出的氢离子数目不同,可将酸分为一元酸、二元酸和多元酸
⑥无氧酸一定是非金属的氢化物.
| A. | ①③④⑤ | B. | ①②④⑥ | C. | ①②③⑥ | D. | ②③⑤⑥ |
1.常温下,往H2O2溶液中滴加少量FeSO4溶液,可发生如下两个反应:
(1)2Fe2++H2O2+2H+═2Fe3++2H2O (2)2Fe3++H2O2═2Fe2++O2↑+2H+
下列说法不正确的是( )
(1)2Fe2++H2O2+2H+═2Fe3++2H2O (2)2Fe3++H2O2═2Fe2++O2↑+2H+
下列说法不正确的是( )
| A. | (1)中H2O2的氧化性比Fe3+强,其还原性比Fe2+弱 | |
| B. | 在反应过程中,溶液的H+浓度不变 | |
| C. | 在反应过程中,Fe2+和Fe3+的总量保持不变 | |
| D. | H2O2生产过程要严格避免混入Fe2+ |
8.防治SO2污染大气,你认为下列吸收剂合理的是( )
| A. | 水 | B. | 汽油 | C. | 硫酸钠 | D. | 碱液 |
18.下列溶液中各微粒的浓度关系正确的是( )
| A. | 0.1 mol•L-1 NaHCO3溶液中:[Na+]+[H+]═[HCO3-]+2[CO32-]+[OH-] | |
| B. | 0.1 mol•L-1Na2S溶液中:2[Na+]═[S2-]+[HS-]+[H2S] | |
| C. | 0.1 mol•L-1 NaHSO4溶液中:[Na+]>[SO42-]>[H+]>[OH-] | |
| D. | 等体积、等物质的量浓度的乙酸溶液和氢氧化钠溶液混合后:[Na+]=[CH3COO-]>[H+]=[OH-] |
5.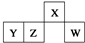 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍.下列判断正确的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍.下列判断正确的是( )
 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍.下列判断正确的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍.下列判断正确的是( )| A. | 原子半径:rW>rZ>rY>rX | |
| B. | 含Y元素的硫酸盐溶液可以和强酸、强碱反应 | |
| C. | 最简单气态氢化物的热稳定性:Z>W | |
| D. | X的氢化物与X的最高价氧化物对应的水化物能形成离子化合物 |
6.实验室测定酸碱反应的反应热时,不需要用到的玻璃仪器是( )
| A. | 试管 | B. | 温度计 | C. | 烧杯 | D. | 环型玻璃搅拌棒 |
7.有关常温下pH均为3的酸酸和硫酸的说法正确的是( )
| A. | 分别加水稀释100倍后,两种溶液的pH仍相同 | |
| B. | 醋酸中的c(CH3COO-)和硫酸中的c(SO42-)相等 | |
| C. | 分别加入足量锌片,两种溶液生成H2的体积相同 | |
| D. | 两种溶液中,由水电离出的氢离子浓度均为1×10-11 mol•L-1 |


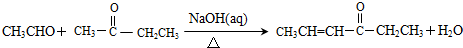
 ,其反应类型是加成反应.
,其反应类型是加成反应.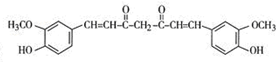 .
.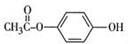 .
.