题目内容
有关物质的量的计算.
(1)有NaCl、CaCl2、AlCl3三种溶液,若溶质的物质的量相等,分别与足量的硝酸银溶液反应,则生成沉淀的物质的量之比为 .若生成的沉淀的质量相等,则三种溶液中溶质的物质的量之比为 .
(2)相同质量的SO2和SO3,所含分子的数目之比为 ;所含O的物质的量之比为 .
(3)下列各物质所含原子数目,按由大到小顺序排列的是
①0.5mol NH3 ②标准状况下22.4L He ③4℃9mL水 ④0.2mol H3PO4.
(1)有NaCl、CaCl2、AlCl3三种溶液,若溶质的物质的量相等,分别与足量的硝酸银溶液反应,则生成沉淀的物质的量之比为
(2)相同质量的SO2和SO3,所含分子的数目之比为
(3)下列各物质所含原子数目,按由大到小顺序排列的是
①0.5mol NH3 ②标准状况下22.4L He ③4℃9mL水 ④0.2mol H3PO4.
考点:物质的量的相关计算
专题:
分析:(1)假设NaCl、CaCl2、AlCl3均为1mol,根据氯离子守恒计算生成AgCl的物质的量之比;
假设AgCl的物质的量为3mol,根据氯离子守恒计算NaCl、CaCl2、AlCl3的物质的量之比;
(2)根据n=
计算相同质量的SO2和SO3的物质的量之比,所含分子的数目之比等于其物质的量之比,结合分子含有氧原子数目计算含有氧原子物质的量之比,含有氧原子质量之比等于其物质的量之比;
(3)根据n=
计算氦气物质的量,根据m=ρV计算水的质量,再根据
计算水的物质的量,结合分子含有原子数目计算各物质含有原子总物质的量.
假设AgCl的物质的量为3mol,根据氯离子守恒计算NaCl、CaCl2、AlCl3的物质的量之比;
(2)根据n=
| m |
| M |
(3)根据n=
| V |
| Vm |
| m |
| M |
解答:
解:(1)假设NaCl、CaCl2、AlCl3均为1mol,根据氯离子守恒,三者生成AgCl的物质的量之比为1mol:2mol:3mol=1:2:3;
假设AgCl的物质的量为3mol,根据氯离子守恒,NaCl、CaCl2、AlCl3的物质的量之比为
:
:
=6:3:2,
故答案为:1:2:3;6:3:2;
(2)根据n=
可知,相同质量的SO2和SO3的物质的量之比为80g/mol:64g/mol=5:4,所含分子的数目之比等于其物质的量之比,即相同质量的SO2和SO3的分子数目之比为5:4,则二者含有氧原子物质的量之比为5×2:4×3=5:6,故二者含有氧原子质量之比为5:6,
故答案为:5:4;5:6;
(3)①0.5mol NH3 含有原子物质的量为0.5mol×4=2mol,②标准状况下22.4L He 的物质的量为1mol,氦气是单原子分子,含有原子为1mol,③4℃9mL水 的质量为9g,其物质的量为
=0.5mol,含有原子物质的量为0.5mol×3=1.5mol,②,④0.2mol H3PO4含有原子物质的量为0.2mol×8=1.6mol,故含有原子数目由大到小的顺序为:①④③②,故答案为:①④③②.
假设AgCl的物质的量为3mol,根据氯离子守恒,NaCl、CaCl2、AlCl3的物质的量之比为
| 3mol |
| 1 |
| 3mol |
| 2 |
| 3mol |
| 3 |
故答案为:1:2:3;6:3:2;
(2)根据n=
| m |
| M |
故答案为:5:4;5:6;
(3)①0.5mol NH3 含有原子物质的量为0.5mol×4=2mol,②标准状况下22.4L He 的物质的量为1mol,氦气是单原子分子,含有原子为1mol,③4℃9mL水 的质量为9g,其物质的量为
| 9g |
| 18g/mol |
点评:本题考查物质的量有关计算,难度不大,(1)中注意利用赋值法与守恒法解答,注意对公式的理解与灵活应用.

练习册系列答案
相关题目
已知在101kPa、298K条件下,2mol氢气燃烧生成水蒸气放出484kJ热量,下列热化学方程式正确的是( )
A、H2O(g)═H2(g)+
| ||
| B、2H2(g)+O2(g)═2H2O(l)△H=-484 kJ?mol-1 | ||
C、H2(g)+
| ||
| D、2H2(g)+O2(g)═2H2O(g)△H=+484 kJ?mol-1 |
在常温、常压下,取下列四种气态烃质量相等,分别在足量的氧气中燃烧,消耗氧气最多的是( )
| A、C4H10 |
| B、C3H8 |
| C、C2H6 |
| D、CH4 |
设阿伏加德罗常数为NA,标准状况下,m g N2气体含有b个分子,则n g N2在相同状态下的体积为 (单位为L)( )
A、
| ||
B、
| ||
C、
| ||
D、
|
在标准状况下,m g气体A与n g气体B的分子数相同,下列说法中不正确的是( )
| A、两种气体A与B的相对分子质量之比为m:n |
| B、同质量气体A与B的分子数之比为m:n |
| C、同温同压下,A、B两气体的密度之比为n:m |
| D、相同状况下,同体积A、B两气体的质量之比为m:n |
在相同的温度和压强下,下列气体的密度最小的是( )
| A、CO2 |
| B、H2 |
| C、O2 |
| D、Cl2 |
如果a g某气体中含有该气体的分子数为b,则c g该气体在标准状况下的体积是(各选项中NA为阿伏加德罗常数)( )
A、
| ||
B、
| ||
C、
| ||
D、
|
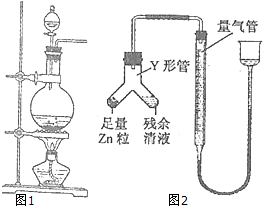 实验室常用MnO2与浓盐酸反应制备Cl2(反应装置如图1示).
实验室常用MnO2与浓盐酸反应制备Cl2(反应装置如图1示).