题目内容
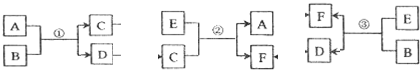
10.已知有以下物质相互转化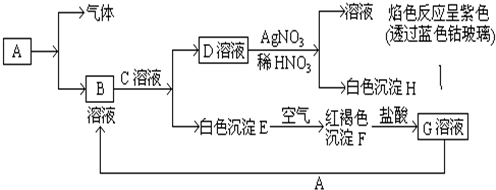
试回答:(1)写出化学式BFeCl2DKClEFe(OH)2FFe(OH)3
(2)写出用KSCN鉴别G溶液的离子方程式Fe3++3SCN-═Fe(SCN)3; 向G溶液加入A的有关离子反应方程式2Fe3++Fe═3Fe2+.
分析 D与硝酸银、硝酸反应得到的溶液,进行焰色反应显紫色,说明D溶液中含有K元素,D能和硝酸银溶液反应生成白色沉淀H为AgCl,所以D是KCl.白色沉淀E在空气中转化为红褐色沉淀F,则E是Fe(OH)2、F是Fe(OH)3,G为FeCl3.B和C反应生成氯化钾和氢氧化亚铁,所以B、C分别是KOH、FeCl2中的一种,G能和A反应生成B,所以A是Fe,B是FeCl2,C是KOH,Fe与盐酸反应得到FeCl2与氢气.
解答 解:D与硝酸银、硝酸反应得到的溶液,进行焰色反应显紫色,说明D溶液中含有K元素,D能和硝酸银溶液反应生成白色沉淀H为AgCl,所以D是KCl.白色沉淀E在空气中转化为红褐色沉淀F,则E是Fe(OH)2、F是Fe(OH)3,G为FeCl3.B和C反应生成氯化钾和氢氧化亚铁,所以B、C分别是KOH、FeCl2中的一种,G能和A反应生成B,所以A是Fe,B是FeCl2,C是KOH,Fe与盐酸反应得到FeCl2与氢气.
(1)由上述分析可知,B为FeCl2,D为KCl,E为Fe(OH)2,F为Fe(OH)3,
故答案为:FeCl2;KCl;Fe(OH)2;Fe(OH)3;
(2)用KSCN鉴别FeCl3溶液的离子方程式:Fe3++3SCN-═Fe(SCN)3,
向FeCl3溶液加入Fe的有关离子反应方程式:2Fe3++Fe═3Fe2+,
故答案为:Fe3++3SCN-═Fe(SCN)3;2Fe3++Fe═3Fe2+.
点评 本题考查无机物推断,试题综合性强,难易适中,焰色反应、反应现象等是推断突破口,侧重对学生基础知识的巩固与训练,熟练掌握元素化合物知识.

练习册系列答案
相关题目
4.下列各种反应类型中,后者一定包含前者的是( )
| A. | 分解复分解 | B. | 氧化化合 | C. | 复分解中和 | D. | 置换氧化还原 |
5.向体积均为10mL且物质的量浓度相同的两份NaOH溶液中分别通入一定量的CO2得到溶液甲和乙;向甲、乙两溶液中分别滴加0.1mol•L-1盐酸,此时反应生成CO2体积(标准状况)与所加盐酸体积间的关系如图所示.则下列叙述中正确的是( )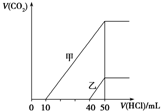

| A. | 原NaOH溶液的物质的量浓度为0.5 mol•L-1 | |
| B. | 当0<V(HCl)<10 mL时,甲溶液中发生反应的离子方程式为:OH-+H+═H2O | |
| C. | 乙溶液中含有的溶质是NaOH、NaHCO3 | |
| D. | 乙溶液中滴加盐酸后产生CO2体积的最大值为112 mL(标准状况) |
2.最近据央视报道,专家选取了我国黑龙江、江西、福建等12个省、市、自治区,采集各种主副食品的烹调方法和食谱,进行了科学细致的检测,结果发现有四成的食品铝含量超过国家标准2到9倍.下列说法中正确的是( )
| A. | 铝的导热性能较好,应大力提倡用铝炊具 | |
| B. | 铝制器具不宜盛放食品较长时间(如放入冰箱中过夜等) | |
| C. | 明矾可用于饮用水的杀菌消毒 | |
| D. | 小孩可以食用含铝较多的食物 |
15.某化学小组设计了如图1所示的数字化实验装置,研究常温下,向1L0.1mol/L H2A溶液中逐滴加入等浓度NaOH溶液时的pH变化情况,并绘制出溶液中含A元素的微粒的物质的量分数与溶液pH的关系如图2所示,则下列说法中正确的是( )
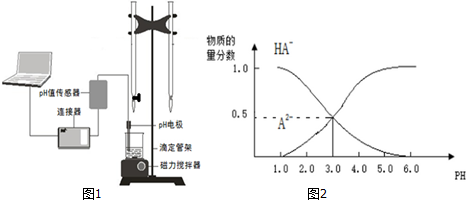

| A. | pH=4.0时,图中n(HA-)约为0.0091mol | |
| B. | 该实验应将左边的酸式滴定管换成右边碱式滴定管并加酚酞作指示剂 | |
| C. | 常温下,等物质的量浓度的NaHA与Na2A溶液等体积混合后溶液pH=3.0 | |
| D. | 0.1mol/LNaHA溶液中存在c(A2-)+c(HA-)+c(H2A)=0.1mol/L |
2.一定量的盐酸跟过量的铁粉反应时,为了减缓反应速度,且不影响生成氢气的总量,可向盐酸中加入适量的( )
| A. | NaOH固体 | B. | NH4Cl固体 | C. | NaNO3固体 | D. | CH3COONa固体 |
19.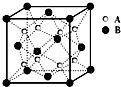 某晶体中晶体结构最小的重复单元如图:A在正方体内,B分别在顶点和面心,则该晶体的化学式为( )
某晶体中晶体结构最小的重复单元如图:A在正方体内,B分别在顶点和面心,则该晶体的化学式为( )
 某晶体中晶体结构最小的重复单元如图:A在正方体内,B分别在顶点和面心,则该晶体的化学式为( )
某晶体中晶体结构最小的重复单元如图:A在正方体内,B分别在顶点和面心,则该晶体的化学式为( )| A. | B2A | B. | BA2 | C. | B7A4 | D. | B4A7 |
 ;反应③的化学方程式为2CO2+2Na2O2=2Na2CO3+O2.
;反应③的化学方程式为2CO2+2Na2O2=2Na2CO3+O2.