题目内容
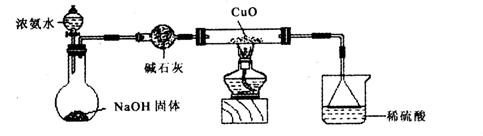
已知NH3具有还原性,与灼热的CuO反应可生成两种单质.某学习小组用下列装置完成并验证该反应.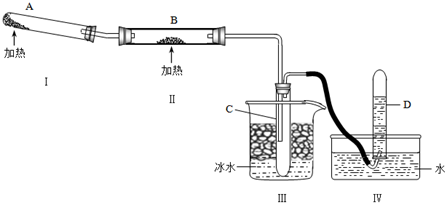
(1)装置Ⅰ的作用是
(2)实验时B中的现象是
(3)设计装置Ⅲ的目的是:
(4)指出整套装置中不完善的地方(指出一处):
分析:(1)分析装置和实验目的可知装置Ⅰ是制备氨气的发生装置,实验室制备氨气的试剂是固体氯化铵和氢氧化钙;
(2)装置B中氨气与灼热氧化铜反应可以生成两种单质,应是氨气还原氧化铜为铜,氨气被还原为氮气,依据原子守恒配平书写化学方程式;
(3)装置Ⅲ目的是冷却生成的水;
(4)装置Ⅰ生成的氨气中含有水蒸气,直接通入装置Ⅱ,容易炸裂玻璃管,需要在ⅠⅡ间增加一个干燥氨气的装置;装置Ⅳ是收集气体装置,易发生倒吸,需要在Ⅲ,Ⅳ之间增加防止倒吸的安全瓶;
(2)装置B中氨气与灼热氧化铜反应可以生成两种单质,应是氨气还原氧化铜为铜,氨气被还原为氮气,依据原子守恒配平书写化学方程式;
(3)装置Ⅲ目的是冷却生成的水;
(4)装置Ⅰ生成的氨气中含有水蒸气,直接通入装置Ⅱ,容易炸裂玻璃管,需要在ⅠⅡ间增加一个干燥氨气的装置;装置Ⅳ是收集气体装置,易发生倒吸,需要在Ⅲ,Ⅳ之间增加防止倒吸的安全瓶;
解答:解:(1)装置Ⅰ是制备氨气的发生装置,实验室制备氨气的试剂是固体氯化铵和氢氧化钙,通过加热反应生成氨气;
故答案为:制备氨气,NH4Cl和Ca(OH)2;
(2)装置B中氨气与灼热氧化铜反应可以生成两种单质,应是氨气还原黑色氧化铜为红色铜,氨气被还原为氮气,反应的化学方程式为:2NH3+3CuO
3Cu+N2+3H2O;
故答案为:黑色粉末变成红色,2NH3+3CuO
3Cu+N2+3H2O;
(3)氨气还原氧化铜反应生成铜、氮气和水,装置Ⅲ目的是冷却生成的水;
故答为:冷凝产物水;
(4)装置Ⅰ生成的氨气中含有水蒸气,直接通入装置Ⅱ,容易炸裂玻璃管,需要在ⅠⅡ间增加一个干燥氨气的装置;
故答案为:装置Ⅰ和Ⅱ之间缺少干燥装置;装置Ⅲ和Ⅳ之间缺少安全瓶;
故答案为:制备氨气,NH4Cl和Ca(OH)2;
(2)装置B中氨气与灼热氧化铜反应可以生成两种单质,应是氨气还原黑色氧化铜为红色铜,氨气被还原为氮气,反应的化学方程式为:2NH3+3CuO
| ||
故答案为:黑色粉末变成红色,2NH3+3CuO
| ||
(3)氨气还原氧化铜反应生成铜、氮气和水,装置Ⅲ目的是冷却生成的水;
故答为:冷凝产物水;
(4)装置Ⅰ生成的氨气中含有水蒸气,直接通入装置Ⅱ,容易炸裂玻璃管,需要在ⅠⅡ间增加一个干燥氨气的装置;
故答案为:装置Ⅰ和Ⅱ之间缺少干燥装置;装置Ⅲ和Ⅳ之间缺少安全瓶;
点评:本题考查了实验室制备氨气的原理和氨气的性质分析判断,实验安全和实验目的理解分析是解题关键,题目难度中等.

练习册系列答案
相关题目