题目内容
2.常温下,某NaOH稀溶液中c(OH-)=10-4 mol•L-1,①此溶液中由水电离产生的c(OH-)是1×10-10mol/L.
②温度不变,将pH=5的硫酸溶液与上述NaOH稀溶液混合后溶液pH变为9,则酸和碱的体积比为9:2.
分析 ①氢氧化钠溶液中,氢氧根离子抑制了水的电离,溶液中氢离子是水电离的;
②pH=5的硫酸溶液中氢离子浓度为1.0×10-5mol/L,pH=9的溶液中氢氧根离子浓度为1.0×10-5mol/L,设出硫酸与氢氧化钠溶液体积,然后列式计算.
解答 解:①常温下,某NaOH稀溶液中c(OH-)=10-4 mol•L-1,氢氧根离子抑制了水的电离,该溶液中的氢离子为水电离的,则此溶液中由水电离产生的c(H+)=c(OH-)=$\frac{1×1{0}^{-14}}{1×1{0}^{-4}}$=1×10-10mol•L-1,
故答案为:1×10-10;
②温度不变,将pH=5的硫酸溶液与上述NaOH稀溶液混合后溶液pH变为9,反应后溶液中氢氧根离子浓度为1.0×10-5mol/L,
设硫酸溶液体积为x,氢氧化钠溶液体积为y,则:$\frac{1{0}^{-4}y-1{0}^{-5}x}{x+y}$=1.0×10-5,整理可得x:y=9:2,即酸和碱的体积比为9:2,
故答案为:9:2.
点评 本题考查了溶液酸碱性与溶液pH的计算,题目难度中等,明确水的电离及其影响为解答关键,注意掌握溶液酸碱性与溶液pH的关系,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
13.下列变化不是由加成反应引起的是( )
| A. | 苯中加溴水振荡,溴水层褪色 | |
| B. | 乙烯通入溴水,溴水褪色 | |
| C. | 石油裂解后的气体通入溴水,溴水褪色 | |
| D. | 苯转化为环己烷 |
17.生活中处处有化学,请你根据所学知识,判断下列说法错误的是( )
| A. | 为防止流感传染,可将教室门窗关闭后,用食醋熏蒸,进行消毒 | |
| B. | 医疗上常用高温煮蒸的方法对医疗器械进行消毒 | |
| C. | 生活中常用在豆浆中加入少量石膏的方法来使豆浆凝固制作豆腐 | |
| D. | 对环境进行消毒的原理是使细菌变性,可以用浓HNO3代替“84”消毒液 |
14.下列叙述Ⅰ和Ⅱ均正确并有因果关系的是( )
| 选项 | 叙述Ⅰ | 叙述Ⅱ |
| A | KNO3的溶解度大 | 用重结晶法除去KNO3中混有的NaCl |
| B | 收集铜与浓硝酸反应生成的气体,用冰水混合物冷却降温,气体颜色变浅 | 生成的红棕色NO2气体部分转化为无色气体 |
| C | 用pH试纸测定NaClO溶液的酸碱性,试纸显蓝色 | NaClO水解显碱性 |
| D | Ca(OH)2能制成澄清石灰水 | 可配制2.0mol•L-1的Ca(OH)2溶液 |
| A. | A | B. | B | C. | C | D. | D |
11.下列转化中,需要加入还原剂才能实现的变化是( )
| A. | S→SO2 | B. | N2→NO | C. | Cl2→NaClO | D. | Fe2(SO4)3→FeSO4 |
12.下列实验操作能达到实验目的是( )
| 选项 | 实验操作 | 实验目的 |
| A | 向含有氯化铁杂质的氯化铜溶液中加入铜 | 除去氯化铁杂质 |
| B | 向某溶液中加入盐酸话的氯化钡溶液 | 效验SO${\;}_{4}^{2-}$的存在 |
| C | 常温下,用pH计测定NaHCO3溶液的pH | 比较HCO${\;}_{3}^{-}$水解、电离程度的相对大小 |
| D | 将SO2通入Ba(NO3)2溶液中 | 证明BaSO3不溶于水 |
| A. | A | B. | B | C. | C | D. | D |
 在100mL NaOH溶液中加入NH4NO3和(NH4)2SO4固体混合物,加热充分反应.加入的混合物质量和产生的气体体积(标准状况)的关系如图.
在100mL NaOH溶液中加入NH4NO3和(NH4)2SO4固体混合物,加热充分反应.加入的混合物质量和产生的气体体积(标准状况)的关系如图. ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种化合价,含ⅥA族元素的化合物在研究和生产中有许多重要用途.请回答下列问题:
ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种化合价,含ⅥA族元素的化合物在研究和生产中有许多重要用途.请回答下列问题: .气态SeO3分子的立体构型为平面三角形,属于非极性(极性、非极性)分子.
.气态SeO3分子的立体构型为平面三角形,属于非极性(极性、非极性)分子.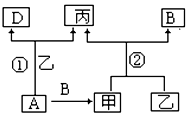 已知A、B、D为单质,其中B、D在常温常压下为气体.甲、乙、丙为常见化合物,甲、丙的焰色反应均为黄色,乙常温下为液体,有关转化关系如图所示:
已知A、B、D为单质,其中B、D在常温常压下为气体.甲、乙、丙为常见化合物,甲、丙的焰色反应均为黄色,乙常温下为液体,有关转化关系如图所示: