题目内容
16.胶状液氢(主要成分是H2和CH4)有望用于未来的运载火箭和空间运输系统.实验测得101kPa时,1mol H2(g)完全燃烧生成液态水,放出285.8kJ的热量;1mol CH4(g)完全燃烧生成液态水和CO2气体,放出890.3kJ的热量.下列热化学方程式书写正确的是( )| A. | 2H2(g)+O2(g)═2H2O(l)△H=-285.8 kJ/mol | |
| B. | CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.3 kJ/mol | |
| C. | CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ/mol | |
| D. | CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=+890.3 kJ/mol |
分析 根据热化学方程式中反应热与物质的物质的量成正比以及热化学方程式的书写方法来解答.
解答 解:1 molH2完全燃烧生成液态水,放出285.8kJ的热量,则热化学方程式为:H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.8 kJ•mol;
1 molCH4完全燃烧生成液态水和CO2,放出890.3kJ的热量,则热化学方程式为:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.3 kJ•mol;
故选B.
点评 本题考查热化学方程式,题目难度不大,做题时要注意热化学方程式中反应热与物质的物质的量成正比以及反应热的符号是否正确.

练习册系列答案
相关题目
6.下列关于反应速率的说法中,错误的是( )
| A. | 反应速率用于衡量化学反应的快慢 | |
| B. | 决定反应速率的主要因素是反应物的性质 | |
| C. | 可逆反应达到化学平衡时,正、逆反应速率都为零 | |
| D. | 化学反应中,纯液体物质不能计算其速率 |
11.按以下实验方案可以从海洋动物柄海鞘中提取具有抗肿瘤活性的天然产物.

下列说法错误的是( )

下列说法错误的是( )
| A. | 步骤①需要使用普通漏斗 | B. | 步骤②要使用分液漏斗 | ||
| C. | 步骤③要用到坩埚 | D. | 步骤④需要蒸馏装置 |
6.常温下,1mol某气态烃CxHy完全燃烧需要氧气5mol,则x与y之和可能是( )
| A. | x+y=5 | B. | x+y=7 | C. | x+y=11 | D. | x+y=13 |
 制取
制取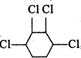 ,即
,即
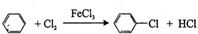 ;⑤
;⑤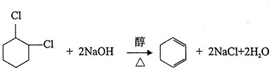 ;⑥
;⑥ .
. .
.
 .
.