题目内容
氮气是制备含氮化合物的一种重要物质,而氮的化合物用途广泛.
(1)下面是利用氮气的一种途径:

①工业上过程Ⅱ的常见化学方程式是 ;
②在碱性溶液中通过电解法可以实现由N2制取NH3:2N2+6H2O
4NH3+3O2,阴极的电极反应式是 .
(2)在25℃下将2a mol?L-1的氨水与0.02mol?L-1的盐酸等体积混合,反应后若溶液显中性,则NH3?H2O的电离常数Kb= .(用含a的代数式表示)
(3)我国化学工程专家侯德榜(1890-1974)于1943年创立的侯氏制碱法,是将氨碱法和合成氨法两种工艺联合起来,同时生产纯碱和氯化铵两种产品的方法.其生产流程可简要表示如图:

①在沉淀池加入饱和食盐水,应先通入的气体是 ;
②沉淀池中反应的化学方程式为 ;
(4)实验室模拟侯氏原理制备纯碱的主要步骤包括:将配制好的饱和NaCl溶液倒人烧杯中,加热到一定温度范围,搅拌下分批加入研细的NH4HCO3固体;加料完毕后,继续保温30min,箭置,过滤得NaHCO3晶体,洗涤晶体,干燥后,转入坩埚中,灼烧2小时,制得Na2CO3晶体.请参考表中的数据填空.
四种盐在不同温度下的溶解度表(g/100g水)
①实验中只析出NaHCO3晶体的原因是 .
②操作过程中反应温度应控制在30℃<t< .
③过滤后得到母液中含有的离子有 ,向其中加入适量盐酸,并做进一步处理,使NaCl循环利用,同时回收NH4Cl.
(1)下面是利用氮气的一种途径:

①工业上过程Ⅱ的常见化学方程式是
②在碱性溶液中通过电解法可以实现由N2制取NH3:2N2+6H2O
| ||
(2)在25℃下将2a mol?L-1的氨水与0.02mol?L-1的盐酸等体积混合,反应后若溶液显中性,则NH3?H2O的电离常数Kb=
(3)我国化学工程专家侯德榜(1890-1974)于1943年创立的侯氏制碱法,是将氨碱法和合成氨法两种工艺联合起来,同时生产纯碱和氯化铵两种产品的方法.其生产流程可简要表示如图:

①在沉淀池加入饱和食盐水,应先通入的气体是
②沉淀池中反应的化学方程式为
(4)实验室模拟侯氏原理制备纯碱的主要步骤包括:将配制好的饱和NaCl溶液倒人烧杯中,加热到一定温度范围,搅拌下分批加入研细的NH4HCO3固体;加料完毕后,继续保温30min,箭置,过滤得NaHCO3晶体,洗涤晶体,干燥后,转入坩埚中,灼烧2小时,制得Na2CO3晶体.请参考表中的数据填空.
四种盐在不同温度下的溶解度表(g/100g水)
| 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
| NH4HCO2 | 11.9 | 15.8 | 21.0 | 27.0 | -* | - |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
②操作过程中反应温度应控制在30℃<t<
③过滤后得到母液中含有的离子有
考点:纯碱工业(侯氏制碱法)
专题:元素及其化合物,化学应用
分析:(1)①氮的固定是将空气中游离态的氮转化为含氮化合物的过程;
②根据电解时阴极物质得到电子,化合价升高,发生还原反应,阳极物质失去电子发生氧化反应;
(2)依据溶液中存在的电荷守恒判断溶液酸碱性;根据溶液的电荷守恒判断,结合NH3?H2O的电离常数Kb=
计算.
(3)①氨气极易溶于水,二氧化碳在水中的溶解度较小;
②饱和食盐水中通入氨气和二氧化碳析出碳酸氢钠晶体;根据过滤的原理和适用范围回答;
析出碳酸氢钠后的溶液为碳酸氢钠的饱和溶液,所以母液中有未反应完的氯化钠和碳酸氢氨,及生成的氯化铵和没有析出的碳酸氢钠;
(4)①根据同温下各物质的溶解度大小来回答;
②碳酸氢铵与碳酸氢钠的溶解度在30℃时相差较大,若温度过低,则反应速率较慢,高于35℃时NH4HCO3开始分解;
③根据所得的母液主要成分来确定其中含有的离子.
②根据电解时阴极物质得到电子,化合价升高,发生还原反应,阳极物质失去电子发生氧化反应;
(2)依据溶液中存在的电荷守恒判断溶液酸碱性;根据溶液的电荷守恒判断,结合NH3?H2O的电离常数Kb=
| c(NH4+)?c(OH-) |
| c(NH3?H2O) |
(3)①氨气极易溶于水,二氧化碳在水中的溶解度较小;
②饱和食盐水中通入氨气和二氧化碳析出碳酸氢钠晶体;根据过滤的原理和适用范围回答;
析出碳酸氢钠后的溶液为碳酸氢钠的饱和溶液,所以母液中有未反应完的氯化钠和碳酸氢氨,及生成的氯化铵和没有析出的碳酸氢钠;
(4)①根据同温下各物质的溶解度大小来回答;
②碳酸氢铵与碳酸氢钠的溶解度在30℃时相差较大,若温度过低,则反应速率较慢,高于35℃时NH4HCO3开始分解;
③根据所得的母液主要成分来确定其中含有的离子.
解答:
解:(1)①氮的固定是将空气中游离态的氮转化为含氮化合物的过程,过程Ⅱ的化学方程式为:N2+O2
2NO,故答案为:N2+O2
2NO;
②阴极N2得到电子,化合价升高,发生还原反应,阳极OH-失去电子发生氧化反应,阴极反应:N2+6e-+6H2O=2 NH3+6OH-,故答案为:N2+6e-+6H2O=2 NH3+6OH-;
(2)反应后溶液中存在电荷守恒:c(NH4+)+c(H+)=c(Cl-)+c(OH-),因为c(NH4+)=c(Cl-),所以c(H+)=c(OH-),溶液呈中性;由溶液的电荷守恒可得:c(H+)+c(NH4+)=c(Cl-)+c(OH-),已知c(NH4+)=c(Cl-),则有c(H+)=c(OH-),所以溶液显中性;平衡时溶液中c(NH4+)=c(Cl-)=0.01mol/L,根据物料守恒得n(NH3.H2O)=(a-0.01)mol/L,根据电荷守恒得c(H+)=c(OH-)=10-7mol/L,电离常数只与温度有关,则此时NH3?H2O的电离常数Kb=
=
=
,故答案为:
;
(3)①二氧化碳在水中的溶解度较小,氨气极易溶于水,所以应该先通氨气有利于吸收二氧化碳,
故答案为:NH3;
②氨气、二氧化碳、水和氯化钠发生反应生成碳酸氢钠和氯化铵,反应方程式为NH3+H2O+CO2+NaCl═NH4Cl+NaHCO3↓,故答案为:NH3+CO2+NaCl+H2O═NaHCO3↓+NH4Cl;
(4)①根据表中数据知道:在相同的温度下,碳酸氢钠的溶解度较小,所以实验中只析出NaHCO3晶体,故答案为:在相同的温度下,碳酸氢钠的溶解度较小;
②碳酸氢铵与碳酸氢钠的溶解度在30℃时相差较大,有利于碳酸氢钠析出,若温度过低,则反应速率较慢,高于35℃时NH4HCO3开始分解,故反应温度控制在30~35℃之间为宜;故答案为:35℃;
③过滤除去析出的碳酸氢钠,溶液中还有部分碳酸氢钠未析出,是碳酸氢钠的饱和溶液,还有溶解在溶液中未析出的NaCl、NH4Cl、NH4HCO3,所得的母液主要成分为NaHCO3、NaCl、NH4Cl、NH4HCO3,Na+、Cl-、HCO3-、NH4+.
故答案为:Na+、Cl-、HCO3-、NH4+.
| ||
| ||
②阴极N2得到电子,化合价升高,发生还原反应,阳极OH-失去电子发生氧化反应,阴极反应:N2+6e-+6H2O=2 NH3+6OH-,故答案为:N2+6e-+6H2O=2 NH3+6OH-;
(2)反应后溶液中存在电荷守恒:c(NH4+)+c(H+)=c(Cl-)+c(OH-),因为c(NH4+)=c(Cl-),所以c(H+)=c(OH-),溶液呈中性;由溶液的电荷守恒可得:c(H+)+c(NH4+)=c(Cl-)+c(OH-),已知c(NH4+)=c(Cl-),则有c(H+)=c(OH-),所以溶液显中性;平衡时溶液中c(NH4+)=c(Cl-)=0.01mol/L,根据物料守恒得n(NH3.H2O)=(a-0.01)mol/L,根据电荷守恒得c(H+)=c(OH-)=10-7mol/L,电离常数只与温度有关,则此时NH3?H2O的电离常数Kb=
| c(NH4+)?c(OH-) |
| c(NH3?H2O) |
| 1×10-7mol/L |
| (a-0.01)mol/L |
| 10-7 |
| a-0.01 |
| 10-7 |
| a-0.01 |
(3)①二氧化碳在水中的溶解度较小,氨气极易溶于水,所以应该先通氨气有利于吸收二氧化碳,
故答案为:NH3;
②氨气、二氧化碳、水和氯化钠发生反应生成碳酸氢钠和氯化铵,反应方程式为NH3+H2O+CO2+NaCl═NH4Cl+NaHCO3↓,故答案为:NH3+CO2+NaCl+H2O═NaHCO3↓+NH4Cl;
(4)①根据表中数据知道:在相同的温度下,碳酸氢钠的溶解度较小,所以实验中只析出NaHCO3晶体,故答案为:在相同的温度下,碳酸氢钠的溶解度较小;
②碳酸氢铵与碳酸氢钠的溶解度在30℃时相差较大,有利于碳酸氢钠析出,若温度过低,则反应速率较慢,高于35℃时NH4HCO3开始分解,故反应温度控制在30~35℃之间为宜;故答案为:35℃;
③过滤除去析出的碳酸氢钠,溶液中还有部分碳酸氢钠未析出,是碳酸氢钠的饱和溶液,还有溶解在溶液中未析出的NaCl、NH4Cl、NH4HCO3,所得的母液主要成分为NaHCO3、NaCl、NH4Cl、NH4HCO3,Na+、Cl-、HCO3-、NH4+.
故答案为:Na+、Cl-、HCO3-、NH4+.
点评:本题考查了联碱法和氨碱法生产流程的原理比较和物质分析判断,明确碳酸钠、碳酸氢钠、氨气、二氧化碳的性质,掌握工艺流程和反应原理是解题关键,题目难度中等.

练习册系列答案
 步步高达标卷系列答案
步步高达标卷系列答案
相关题目
垃圾分类从你我他开始.废弃塑料瓶属于( )
A、 |
B、 |
C、 |
D、 |
下列有关物质的性质与应用均正确的是( )
| A、Na2O2是碱性氧化物,具有强氧化性可用于杀菌消毒 |
| B、胶体与溶液的本质区别是能否出现丁达尔现象 |
| C、Al2O3是难熔的物质,可制造耐火坩埚 |
| D、小苏打能与酸反应,医疗上可以治疗胃溃疡 |
下列反应所得溶液中一定只含一种溶质的是( )
| A、向稀硝酸中加入铁粉 |
| B、向氯化铝溶液中加入过量的氨水 |
| C、向NaOH溶液中通入CO2气体 |
| D、向MgSO4、H2SO4的混合液中加入过量的Ba(OH)2溶液 |
下列反应离子方程式正确的是( )
| A、大理石溶于醋酸溶液:CaCO3+2H+═Ca2++CO2↑+H2O |
| B、氯气通入冷的氢氧化钠溶液中:2Cl2+2OH-=3Cl-+ClO-+H2O |
| C、向澄清石灰水中加入少量小苏打溶液:Ca2++OH-+HCO3-=CaCO3↓+H2O |
| D、氨水中通入过量二氧化硫:2NH3?H2O+SO2=2NH4++SO32-+2H2O |


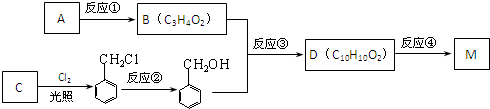
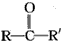 (R、R’代表烷基或H原子)发生缩合反应生成新的有机物和水.苯酚还能发生如图1反应生成有机酸酯:
(R、R’代表烷基或H原子)发生缩合反应生成新的有机物和水.苯酚还能发生如图1反应生成有机酸酯: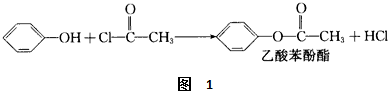
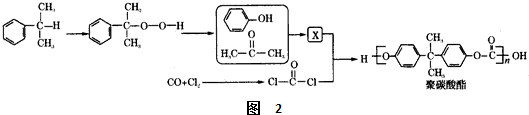
 反应合成聚碳酸酯的化学方程式
反应合成聚碳酸酯的化学方程式