题目内容
7.(1)标准状况下,11.2L HCL气体溶于水,制成200mL盐酸,所得溶液中氯化氢的物质的量浓度为2.5mol/L;将上述溶液稀释成1L溶液稀释成溶液甲,则其氯化氢的物质的量浓度为0.5mol/L.(2)从溶液甲中取出250mL盐酸与足量铁反应,标准状况下可生成多少体积气体?(很锯化学方程式计算)
分析 (1)依据n=$\frac{V}{Vm}$,c=$\frac{n}{V}$,依据溶液稀释过程中溶质的物质的量不变计算稀释后溶液浓度;
(2)根据氢原子守恒计算出生成氢气的物质的量,再根据V=nVm计算出标况下氢气的体积.
解答 解:(1)标准状况下,11.2L HCL气体物质的量为:$\frac{11.2L}{22.4L/mol}$=0.5mol,制成200mL盐酸,所得溶液中氯化氢的物质的量浓度为:$\frac{0.5mol}{0.2L}$=2.5mol/L,将上述溶液稀释成1L溶液稀释成溶液甲,设稀释后溶液浓度为C,则依据溶液稀释过程中溶质的物质的量不变得:2.5mol/L×200mL=1000mL×C,解得C=0.5mol/L;
故答案为:2.5mol/L;0.5mol/L;
(2)250mL 0.5mol/L的该盐酸中含有氯化氢的物质的量为:n(HCl)=0.5mol/L×0.25L=0.125mol,根据方程式:Fe+2HCl=FeCl2+H2↑,结合氢元素质量守恒,0.125molHCl完全反应生成氢气的物质的量为:$\frac{1}{2}$×0.125mol=0.0625mol,标况下体积为:0.0625mol×22.4L/mol=1.4L;
故答案为:标准状况下可生成1.4L体积气体.
点评 本题考查了物质的量有关计算,明确物质的量浓度概念及溶液稀释规律是 解题关键,题目难度不大.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
17.下列离子方程式中,正确的是( )
| A. | 氢氧化钠溶液中通入过量CO2:CO2+2OH-═CO${\;}_{3}^{2-}$+H2O | |
| B. | 向澄清石灰水中通入过量CO2;Ca2++2OH-+CO2=CaCO3↓++H2O | |
| C. | 硫酸氢钠溶液中加入过量氢氧化钡溶液:2HSO${\;}_{4}^{-}$+2Ba2++2OH-=2BaSO4↓+2H2O | |
| D. | 向碳酸氢钙溶液中加入过量石灰水:Ca2++OH-+HCO${\;}_{3}^{-}$=CaCO3↓+H2O |
18.物质应用与其性质密切相关,下列说法错误的是( )
| A. | 硅胶可防止食物受潮是由于其具有吸水性 | |
| B. | 葡萄糖用于医疗输液是因为它属于强电解质 | |
| C. | Na2CO3可用作食用碱,因为Na2CO3的水溶液显碱性 | |
| D. | 酸性重铬酸钾用于检查酒驾是利用其强氧化性 |
12.绿矾(FeSO4•7H2O)是治疗缺铁性贫血药品的重要成分.如图是以市售铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法:
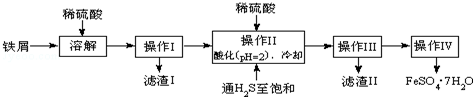
查询资料,得有关物质的数据如下:
(1)加稀硫酸的溶解中,铁作还原剂的离子方程式为Fe+2H+=Fe2++H2↑、2Fe3++Fe=3Fe2+.
(2)操作Ⅱ中:
①通入硫化氢至饱和的目的是a除去溶液中的Sn2+离子;b防止Fe2+被氧化;
②在溶液中用硫酸酸化至pH=2的目的是防止Fe2+离子生成沉淀.
(3)操作IV的顺序依次为蒸发浓缩、冷却结晶、过滤、洗涤.

查询资料,得有关物质的数据如下:
| 25℃时 | pH值 | 25℃时 | pH值 |
| 饱和H2S溶液 | 3.9 | FeS开始沉淀 | 3.0 |
| SnS沉淀完全 | 1.6 | FeS沉淀完全 | 5.5 |
(2)操作Ⅱ中:
①通入硫化氢至饱和的目的是a除去溶液中的Sn2+离子;b防止Fe2+被氧化;
②在溶液中用硫酸酸化至pH=2的目的是防止Fe2+离子生成沉淀.
(3)操作IV的顺序依次为蒸发浓缩、冷却结晶、过滤、洗涤.
2.CO是生产羰基化学品的基本原料,对于以水煤气为原料提取CO的工艺,如果氢气未能充分利用,则提高了CO生产成本,所以在煤化工中常需研究不同温度下的平衡常数、投料比及热值问题.反应CO(g)+H2O (g)?H2(g)+CO2(g)的平衡常数随温度的变化如下表:
(1)上述反应的正反应是放热(填“放热”或“吸热”)反应.
(2)已知在一定温度下:C(s)+CO2(g)?2CO(g) K
C(s)+H2O (g)?H2(g)+CO(g) K1
CO(g)+H2O (g)?H2(g)+CO2(g) K2
则K、K1、K2、之间的关系是K=$\frac{{K}_{1}}{{K}_{2}}$.
(3)800℃时,在2L的恒容密闭容器中,充入2.0molCO(g)和3.0molH2O(g),保持温度不变进行反应:CO(g)+H2O (g)?H2(g)+CO2(g),4min时反应达到平衡,测得CO的转化率为60%.
①0~4min内,CO2的平均反应速率为0.15mol•L-1•min-1,800℃时a=1.
②800℃时四个不同容器中发生上述反应,测得各物质的浓度(mol•L-1)如下
表,其中达到平衡的是D(填字母).
(4)向某密闭容器中充入1molCO和2molH2O(g),发生反应:CO(g)+H2O (g)?H2(g)+CO2(g).当反应达到平衡时,CO的体积分数为x.若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达到平衡时CO的体积分数大于x的是B
A、0.5molCO+2molH2O(g)+1molCO2+1molH2
B、1molCO+1molH2O(g)+1molCO2+1molH2
C、0.5molCO+1.5molH2O(g)+0.4molCO2+0.4molH2
D、0.5molCO+1.5molH2O(g)+0.5molCO2+0.5molH2.
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | a |
(2)已知在一定温度下:C(s)+CO2(g)?2CO(g) K
C(s)+H2O (g)?H2(g)+CO(g) K1
CO(g)+H2O (g)?H2(g)+CO2(g) K2
则K、K1、K2、之间的关系是K=$\frac{{K}_{1}}{{K}_{2}}$.
(3)800℃时,在2L的恒容密闭容器中,充入2.0molCO(g)和3.0molH2O(g),保持温度不变进行反应:CO(g)+H2O (g)?H2(g)+CO2(g),4min时反应达到平衡,测得CO的转化率为60%.
①0~4min内,CO2的平均反应速率为0.15mol•L-1•min-1,800℃时a=1.
②800℃时四个不同容器中发生上述反应,测得各物质的浓度(mol•L-1)如下
表,其中达到平衡的是D(填字母).
| c(CO2) | 3 | 1 | 0.8 | 1 |
| c(H2) | 2 | 1 | 0.8 | 1 |
| c(CO) | 1 | 2 | 3 | 0.5 |
| c(H2O) | 2 | 2 | 3 | 2 |
A、0.5molCO+2molH2O(g)+1molCO2+1molH2
B、1molCO+1molH2O(g)+1molCO2+1molH2
C、0.5molCO+1.5molH2O(g)+0.4molCO2+0.4molH2
D、0.5molCO+1.5molH2O(g)+0.5molCO2+0.5molH2.
19.25℃时,下列有关电解质溶液说法正确的是( )
| A. | 稀醋酸中加入冰醋酸,醋酸电离平衡右移,电离度增大 | |
| B. | 向NaF溶液中滴加硫酸至中性时,c(SO42-)<c(HF) | |
| C. | 向氨水中加入NH4C1固体,溶液中$\frac{c(N{H}_{3}•{H}_{2}O)•c({H}^{+})}{c(N{H}_{4}^{+})}$增大 | |
| D. | AgCl在水和NaCl溶液中的溶度积分别为K1、K2,则K1>K2 |
20.过氧化钠是一种制氧剂,它和二氧化碳反应方程式为:2Na2O2+2CO2→2Na2CO3+O2下列说法正确的是( )
| A. | Na2O2是氧化剂,CO2是还原剂 | |
| B. | Na2CO3是还原产物,O2是氧化产物 | |
| C. | 每转移4摩尔电子,有1摩尔氧气生成 | |
| D. | 1摩尔CO2参加反应就会产生11.2LO2 |