题目内容
15.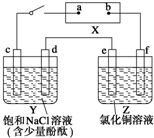 如图中X是直流电源.Y槽中c、d为石墨棒,Z槽中e、f是质量相同的铜棒.接通电路后,发现d附近显红色.
如图中X是直流电源.Y槽中c、d为石墨棒,Z槽中e、f是质量相同的铜棒.接通电路后,发现d附近显红色.(1)①电源上b为负极.
②Z槽中e为阳极.
③连接Y、Z槽线路中,电子流动的方向是d←e(用“→”或“←”填空).
(2)①写出c极上反应的电极反应式2Cl--2e-=Cl2↑.
②写出Y槽中总反应化学方程式2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑.
③写出Z槽中e极上反应的电极反应式Cu-2e-═Cu2+.
(3)①电解2min后,取出e、f,洗净、烘干、称量,质量差为2.56g,在通电过程中,电路中通过的电子为0.04mol.
②若Y槽中溶液体积为100mL(电解后可视为不变),槽中电解反应的速率v(OH-)=0.2 mol•L-1•min-1.
分析 X为直流电源,Y槽中c、d为石墨棒,Z槽中e、f是质量相同的铜棒,接通电路后发现d附近显红色,则d附近生成氢氧根离子,则d极为电解池阴极,d电极上氢离子放电生成氢气和氢氧根离子,c为阳极,c电极上氯离子放电,则a是直流电源正极,b是直流电源负极;电子从原电池的负极流向电解池的阴极,再到阳极,最后流入原电池的正极;结合电解池中两极上的反应分析
解答 解:X为直流电源,Y槽中c、d为石墨棒,Z槽中e、f是质量相同的铜棒,接通电路后发现d附近显红色,则d附近生成氢氧根离子,则d极为电解池阴极,d电极上氢离子放电生成氢气和氢氧根离子,c为阳极,c电极上氯离子放电,则a是直流电源正极,b是直流电源负极
(1)①由以上分析可知b为负极,故答案为:负;
②Z槽中e与原电池正极相连为阳极;故答案为:阳;
③连接Y、Z槽线路中,电子流动的方向是从e流向d,故答案为:←;
(2)①c为阳极,c电极上氯离子放电,c极上反应的电极反应式为:2Cl--2e-=Cl2↑,故答案为:2Cl--2e-=Cl2↑;
②Y槽中为惰性电极电解氯化钠溶液,其总反应的化学方程式为2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑,
故答案为:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑;
③Z槽中e极与电源正极相连为阳极,其电极反应式为Cu-2e-═Cu2+,故答案为:Cu-2e-═Cu2+.
(3)①设电路中转移的电子为xmol,根据e极:Cu-2e-=Cu2+,△m=64 得e极质量减轻:32x(g);
f极:Cu2++2e-=Cu,△m=64 得f极质量增重:32x(g),所以有:32x+32x=2.56,得x=0.04mol,
故答案为:0.04;
②因为两槽是串联,电极上流过的电量相等,在电解氯化钠溶液中,每流过1mol电子,溶液中就会产生1mol氢氧根离子,根据①可知,2min流过0.04mol电子,所以每分钟溶液中产生的氢氧根的物质的量为0.02mol,所以槽中电解反应的速率v(OH-)=$\frac{\frac{0.02mol}{0.1L}}{1min}$0.2mol/(L•min),故答案为:0.2 mol•L-1•min-1.
点评 本题考查学生电解池的工作原理知识,明确图中电源的正负极确定以及电解池的阴阳极上的反应是解答的关键,并熟悉电极反应及离子的放电顺序来解答,题目难度中等.

 氧元素和卤族元素都能形成多种物质,我们可以利用所学物质结构与性质的相关知识去认识和理解.
氧元素和卤族元素都能形成多种物质,我们可以利用所学物质结构与性质的相关知识去认识和理解.(1)COCl2 的空间构型为平面三角形;溴的基态原子价电子排布式为4s24p5.
(2)已知CsICl2不稳定,受热易分解,倾向于生成晶格能更大的物质,则它按下列A式发生(填字母代号,下同).
A.CsICl2═CsCl+ICl B.CsICl2═CsI+Cl2?
(3)根据下表提供的第一电离能数据判断,最有可能生成较稳定的单核阳离子的卤素原子是碘(或I).
| 氟 | 氯 | 溴 | 碘 | |
(kJ/mol) | 1681 | 1251 | 1140 | 1008 |
A.HCl B.HF C.SO2 D.SCl2
(5)已知ClO2-为三角形,中心氯原子周围有四对价层电子.ClO3- 中心氯原子的杂化轨道类型为sp3杂化,写出一个与CN-互为等电子体的物质的分子式N2或CO.
(6)钙在氧气中燃烧时得到一种钙的氧化物晶体,其结构如图所示,由此可判断钙的氧化物的化学式为CaO2.已知该氧化物的密度是ρ g/cm3,则晶胞内离得最近的两个钙离子的间距为$\frac{\sqrt{2}}{2}×\root{3}{\frac{72×4}{ρ{N}_{A}}}$cm(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA).
| A. | 向某溶液中加入稀盐酸,产生无色无味且能使石灰水变浑浊的气体,该溶液一定含有CO32- | |
| B. | 用洁净的铂丝蘸取少量某溶液在无色火焰上灼烧,火焰呈黄色,该溶液一定是钠盐溶液 | |
| C. | 向某溶液中加入BaCl2溶液,有沉淀生成,再加入稀盐酸,沉淀不消失,该溶液一定含有SO42- | |
| D. | 向某溶液中滴加KSCN 溶液,溶液不变色,滴加氯水后溶液显红色,该溶液中一定含Fe2+ |
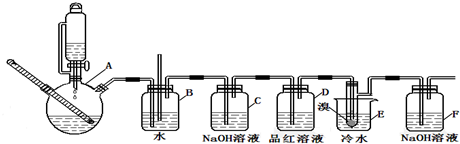
有关数据列表如下:
| 乙醇 | 1,2二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g/cm2 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
(1)A中药品为1:3的无水乙醇和浓硫酸混合液,写出制备乙烯的化学反应方程式:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O.
(2)请写出C装置中的作用除去乙烯中混有的酸性气体杂质.
(3)反应过程中应用冷水冷却装置E,其主要目的是减少液溴挥发;
(4)学生发现反应结束时,无水乙醇消耗量大大超过理论值,其原因是乙醇挥发、副反应发生或反应太剧烈.
(5)有学生提出,装置F中可改用足量的四氯化碳液体吸收多余的气体,判断改用四氯化碳液体是否可行是(填“是”或“否”),其原因是乙烯和液溴均易溶于四氯化碳.
(6)制取的1,2-二溴乙烷可以进一步反应生成一种有机物,汽车常用该有机物作为防冻液.写出由1,2-二溴乙烷制取该有机物的反应方程式:BrCH2BrCH2Br+2NaOH$→_{△}^{水}$HOCH2CH2OH+2NaBr,反应类型水解反应或取代反应.
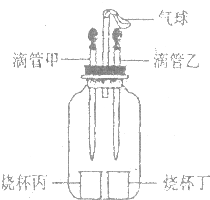 如图所示装置(气密性良好),若先将甲中液体挤出,观察到气球明显鼓起,一段时间后恢复原状;再将乙中液体挤出,气球又明显鼓起.下列组合正确的是( )
如图所示装置(气密性良好),若先将甲中液体挤出,观察到气球明显鼓起,一段时间后恢复原状;再将乙中液体挤出,气球又明显鼓起.下列组合正确的是( )| 选项 | 滴管甲 | 烧杯丙 | 滴管乙 | 烧杯丁 |
| A | 双氧水 | 二氧化锰 | 水 | 氢氧化钠 |
| B | 盐酸 | 镁 | 盐酸 | 碳酸纳 |
| C | 水 | 氢氧化钠 | 水 | 硝酸铵 |
| D | 水 | 氧化钙 | 盐酸 | 镁 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 乙醇和乙酸都是常用调味品的主要成分 | |
| B. | 通过红外光谱分析可以区分乙醇与乙酸乙酯 | |
| C. | 溴丙烷水解制丙醇与丙烯和水反应制丙醇属于不同反应类型 | |
| D. | 乙醇和乙酸之间能发生酯化反应,酯化反应和皂化反应互为逆反应 |
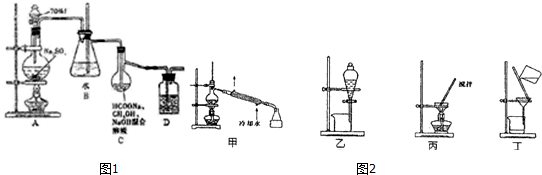
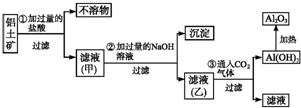 工业上用铝土矿(主要成分SiO2、Al2O3、Fe3O4)提取氧化铝作冶炼铝的原料,提取的操作过程如图所示:
工业上用铝土矿(主要成分SiO2、Al2O3、Fe3O4)提取氧化铝作冶炼铝的原料,提取的操作过程如图所示: .
.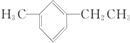 名称为1-甲基-3-乙基苯.
名称为1-甲基-3-乙基苯.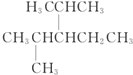 名称为:2,4-二甲基-3-乙基戊烷.
名称为:2,4-二甲基-3-乙基戊烷.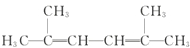 名称为:2,5-二甲基-2,4-己二烯.
名称为:2,5-二甲基-2,4-己二烯. ;
;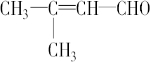 .
.