��Ŀ����
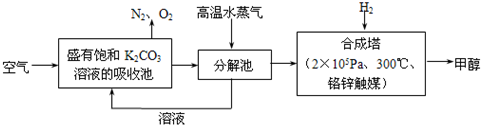
Ϊ��С������CO2�Ի�����Ӱ�죬�п�ѧ���������ɫ���ɡ����룮���Ȱѿ�������̼�����Һ��Ȼ���ٰ�CO2����Һ����ȡ��������ʹ֮��Ϊ������ȼ�ϼ״�������ɫ���ɡ����뼼���������£�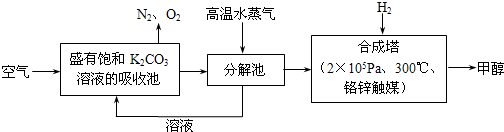
��1��д���ֽ���з�Ӧ�Ļ�ѧ����ʽ______��
��2���ںϳ����У�����4.4kg CO2������H2��ȫ��Ӧ���ɷ���4947kJ��д���ϳ����з�Ӧ���Ȼ�ѧ����ʽ______��
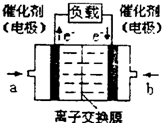
��3��д������������Ϊ����ʵļ״�ȼ�ϵ�صĸ�����Ӧʽ______��
������ת��Ϊ______ molʱ���μӷ�Ӧ�������������6.72L����״���£���
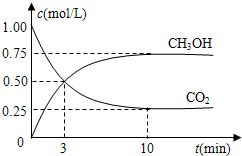
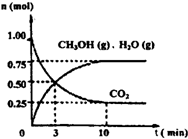
��4�����ݻ�Ϊ1L���ܱ������У�����1mol CO2��3mol H2����500���·�����Ӧ���й����ʵ�Ũ����ʱ��仯��ͼ��ʾ��
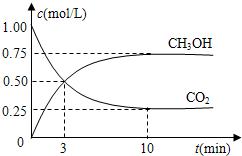
�ٴӷ�Ӧ��ʼ��ƽ�⣬H2��ƽ����Ӧ����v��H2��=______��
���������������䣬ֻ���¶���ߵ�800�棬�ٴδ�ƽ��ʱ��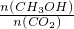 ��ֵ______�����������С�����䡱����
��ֵ______�����������С�����䡱����
�⣺��1��������̼�ͱ��͵�̼�����Һ��Ӧ����̼����أ�̼����ز��ȶ�������ʱ�ֽ�����̼��ء�������̼��ˮ�����Է���ʽΪ2KHCO3 K2CO3+H2O+CO2����
K2CO3+H2O+CO2����
�ʴ�Ϊ��2KHCO3 K2CO3+H2O+CO2����
K2CO3+H2O+CO2����
��2��4.4kgCO2�����ʵ�����100mol��100mol������̼������������Ӧ�ų�4947KJ����������1mol������̼������������Ӧ�ų�49.47KJ�������������Ȼ�ѧ��Ӧ����ʽΪCO2��g��+3H2��g��=CH3OH��g��+H2O��g����H=-49.47KJ/mol��
�ʴ�Ϊ��CO2��g��+3H2��g��=CH3OH��g��+H2O��g����H=-49.47KJ/mol��
��3���״�ȼ�ϼ��Ե���У��״��ڸ����Ϸ���������Ӧ���״�ʧ���Ӻ����������ӷ�Ӧ����̼������Ӻ�ˮ���缫��ӦʽΪCH3OH+8OH--6e-=CO32-+6H2O���μӷ�Ӧ�������������6.72L����״���£����ʵ���Ϊ0.3mol��O2+2H2O+4e-=4OH-��ת�Ƶ������ʵ���Ϊ1.2mol��
�ʴ�Ϊ��CH3OH+8OH--6e-=CO32-+6H2O�� 1.2��
��4����ͼ��������״���ʾ�ķ�Ӧ����=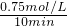 =0.075mol/L?min�����ݻ�ѧ����ʽCO2��g��+3H2��g��=CH3OH��g��+H2O��g������õ�������ʾ�ķ�Ӧ����=0.075mol/L?min��3=0.225 mol/��L?min����
=0.075mol/L?min�����ݻ�ѧ����ʽCO2��g��+3H2��g��=CH3OH��g��+H2O��g������õ�������ʾ�ķ�Ӧ����=0.075mol/L?min��3=0.225 mol/��L?min����
�ʴ�Ϊ��0.225 mol/��L?min����
�ڷ�Ӧ�Ƿ��ȷ�Ӧ���������������䣬ֻ���¶���ߵ�800�棬ƽ��������У��ٴδ�ƽ��ʱ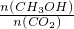 ��ֵ��С��
��ֵ��С��
�ʴ�Ϊ����С��
��������1��̼����ز��ȶ�������ʱ�ֽ�����̼��غͶ�����̼��ˮ��
��2��4.4kgCO2�����ʵ�����100mol��100mol������̼������������Ӧ�ų�4947KJ����������1mol������̼������������Ӧ�ų����������Ӷ�д�����Ȼ�ѧ��Ӧ����ʽ��
��3���״�ȼ�ϵ���У������ϼ״�ʧȥ���ӷ���������Ӧ�������������õ��ӷ�����ԭ��Ӧ��
��4�������ݻ�ѧ��Ӧ���ʵĸ�����㣬�õ�λʱ��������Ũ�ȵı仯����õ���
�ڷ�Ӧ�Ƿ��ȷ�Ӧ�¶�����ƽ��������У�
���������⿼���˹�ҵ�Ʊ����ʵ�ԭ��Ӧ�ã��Ȼ�ѧ����ʽ����д������ע�����⣬ԭ���ԭ��Ӧ�ã���ѧ��Ӧ���ʼ����ƽ��Ӱ�����ص����⣬��Ŀ�Ѷ��еȣ�
 K2CO3+H2O+CO2����
K2CO3+H2O+CO2�����ʴ�Ϊ��2KHCO3
 K2CO3+H2O+CO2����
K2CO3+H2O+CO2������2��4.4kgCO2�����ʵ�����100mol��100mol������̼������������Ӧ�ų�4947KJ����������1mol������̼������������Ӧ�ų�49.47KJ�������������Ȼ�ѧ��Ӧ����ʽΪCO2��g��+3H2��g��=CH3OH��g��+H2O��g����H=-49.47KJ/mol��
�ʴ�Ϊ��CO2��g��+3H2��g��=CH3OH��g��+H2O��g����H=-49.47KJ/mol��
��3���״�ȼ�ϼ��Ե���У��״��ڸ����Ϸ���������Ӧ���״�ʧ���Ӻ����������ӷ�Ӧ����̼������Ӻ�ˮ���缫��ӦʽΪCH3OH+8OH--6e-=CO32-+6H2O���μӷ�Ӧ�������������6.72L����״���£����ʵ���Ϊ0.3mol��O2+2H2O+4e-=4OH-��ת�Ƶ������ʵ���Ϊ1.2mol��
�ʴ�Ϊ��CH3OH+8OH--6e-=CO32-+6H2O�� 1.2��
��4����ͼ��������״���ʾ�ķ�Ӧ����=
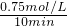 =0.075mol/L?min�����ݻ�ѧ����ʽCO2��g��+3H2��g��=CH3OH��g��+H2O��g������õ�������ʾ�ķ�Ӧ����=0.075mol/L?min��3=0.225 mol/��L?min����
=0.075mol/L?min�����ݻ�ѧ����ʽCO2��g��+3H2��g��=CH3OH��g��+H2O��g������õ�������ʾ�ķ�Ӧ����=0.075mol/L?min��3=0.225 mol/��L?min���� �ʴ�Ϊ��0.225 mol/��L?min����
�ڷ�Ӧ�Ƿ��ȷ�Ӧ���������������䣬ֻ���¶���ߵ�800�棬ƽ��������У��ٴδ�ƽ��ʱ
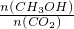 ��ֵ��С��
��ֵ��С���ʴ�Ϊ����С��
��������1��̼����ز��ȶ�������ʱ�ֽ�����̼��غͶ�����̼��ˮ��
��2��4.4kgCO2�����ʵ�����100mol��100mol������̼������������Ӧ�ų�4947KJ����������1mol������̼������������Ӧ�ų����������Ӷ�д�����Ȼ�ѧ��Ӧ����ʽ��
��3���״�ȼ�ϵ���У������ϼ״�ʧȥ���ӷ���������Ӧ�������������õ��ӷ�����ԭ��Ӧ��
��4�������ݻ�ѧ��Ӧ���ʵĸ�����㣬�õ�λʱ��������Ũ�ȵı仯����õ���
�ڷ�Ӧ�Ƿ��ȷ�Ӧ�¶�����ƽ��������У�
���������⿼���˹�ҵ�Ʊ����ʵ�ԭ��Ӧ�ã��Ȼ�ѧ����ʽ����д������ע�����⣬ԭ���ԭ��Ӧ�ã���ѧ��Ӧ���ʼ����ƽ��Ӱ�����ص����⣬��Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
�����Ŀ
 ��2012?������ģ����ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2������ȫ������ձ����ӣ�Ϊ��С������CO2�Ի�����Ӱ�죬һ����������������������ŷ�������һ�����ѧ�Ҽ�ǿ�˶�CO2�������õ��о���
��2012?������ģ����ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2������ȫ������ձ����ӣ�Ϊ��С������CO2�Ի�����Ӱ�죬һ����������������������ŷ�������һ�����ѧ�Ҽ�ǿ�˶�CO2�������õ��о���