题目内容
下列化学反应能用离子反应Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O表示的是( )
| A、Ca(OH)2与少量的NaHCO3 |
| B、Ca(OH)2与少量的Ca(HCO3)2 |
| C、Ca(HCO3)2与足量的NaOH |
| D、Ca(OH)2与足量的Ca(HCO3)2 |
考点:离子方程式的书写
专题:离子反应专题
分析:与量有关的离子反应中,量少的物质完全反应,碳酸钙、水在离子反应中保留化学式,以此来解答.
解答:
解:A.Ca(OH)2与少量的NaHCO3反应的离子反应为Ca2++HCO3-+OH-=CaCO3↓+H2O,故A不选;
B.Ca(OH)2与少量的Ca(HCO3)2反应的离子反应为Ca2++HCO3-+OH-=CaCO3↓+H2O,故B不选;
C.Ca(HCO3)2与足量的NaOH反应的离子反应为Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O,故C选;
D.Ca(OH)2与足量的Ca(HCO3)2反应的离子反应为Ca2++HCO3-+OH-=CaCO3↓+H2O,故D不选;
故选C.
B.Ca(OH)2与少量的Ca(HCO3)2反应的离子反应为Ca2++HCO3-+OH-=CaCO3↓+H2O,故B不选;
C.Ca(HCO3)2与足量的NaOH反应的离子反应为Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O,故C选;
D.Ca(OH)2与足量的Ca(HCO3)2反应的离子反应为Ca2++HCO3-+OH-=CaCO3↓+H2O,故D不选;
故选C.
点评:本题考查离子反应的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重与量有关的离子反应考查,注意量少的物质完全反应,题目难度不大.

练习册系列答案
相关题目
下列对于“摩尔”的理解正确的是( )
| A、标况下,1 mol任何物质的体积都约为22.4 L |
| B、22.4 L气体所含分子数一定大于11.2 L气体所含的分子数 |
| C、任何条件下,气体的摩尔体积都是22.4 L |
| D、CO2的摩尔质量是44g/mol |
下列叙述中正确的是( )
| A、等体积pH=3的酸溶液和pH=11的碱溶液相互混合后,溶液的pH一定等于7(25℃) |
| B、固态磷酸是电解质,所以磷酸在熔化时或溶解于水时都能导电 |
| C、锌与pH=3的CH3COOH 溶液反应比pH=4 的盐酸反应剧烈 |
| D、在0.1 mol/L Na2CO3溶液中,2c(Na+)=c(H2CO3)+c(CO32-)+c(HCO3-) |
液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点.一种以肼(N2H4)为燃料的电池装置如装置①.该电池用空气中的氧气作为氧化剂,KOH作为电解质.下列叙述不正确的是( )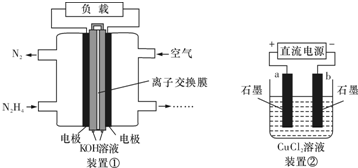

| A、该燃料电池负极发生的电极反应为:N2H4+4OH--4e-═N2+4H2O |
| B、用该燃料电池作为装置②的直流电源,产生1 mol Cl2至少需要通入0.5 mol N2H4 |
| C、该燃料电池的电极材料应采用多孔导电材料,以提高电极反应物质在电极表面的吸附量,并使它们与电解质溶液充分接触 |
| D、该燃料电池中,电子从右侧电极经过外电路流向左侧电极,溶液中OH-则迁移到左侧 |
下列说法中正确的是( )
| A、常温下,某难溶物的Ksp为2.5×105 | ||||
| B、镀铜铁制品镀层受损后,铁制品比受损前更容易生锈 | ||||
C、NH3?H2O溶液加水稀释后,溶液中
| ||||
| D、常温下,pH均为5的盐酸与氯化铵溶液中,水的电离程度相同 |
在地球上空10~50km的大气层中,集结着大量的臭氧分子(O3),形成臭氧层,吸收了太阳光中绝大部分紫外线,使地球上的生物免遭过量紫外线辐射的危害.但空调和冰箱中的制冷剂“氟里昂”(以M代表其化学式),逸散到大气中可破坏臭氧层,其反应过程可简示为:M+O3→MO+O2,MO+O→M+O2,据此判断“氟里昂”在破坏臭氧层的反应中是( )
| A、催化剂 | B、还原剂 |
| C、氧化剂 | D、稳定剂 |
下列物质既不是电解质,又不是非电解质的是( )
| A、BaSO4 |
| B、NH3?H2O |
| C、盐酸 |
| D、乙醇 |