题目内容
下列溶液中的c(Cl-)与50mL 1mol?L-1AlCl3溶液中的c(Cl-)不相等的是( )
| A、150mL 1mol?L-1氯化钠溶液 |
| B、75mL 1.5 mol?L-1氯化钙溶液 |
| C、150mL 3 mol?L-1氯化钾溶液 |
| D、75mL 1 mol?L-1氯化铁溶液 |
考点:物质的量浓度的相关计算
专题:物质的量浓度和溶解度专题
分析:50mL1mol/L的AlCl3溶液中的Cl-浓度为3mol/L,根据溶质化学式计算各选项中的Cl-物质的量,进行比较可知.注意溶液中溶质离子的浓度与溶液体积无关,只取决于物质电离出的离子的数目多少与溶质的浓度,以此解答.
解答:
解:50mL1mol/L的AlCl3溶液中的Cl-浓度为3mol/L.
A、150ml1mol/L的NaCl溶液中Cl-浓度为1mol/L,与50mL1mol/L的AlCl3溶液中的Cl-浓度不相等,故A选;
B、75mL 1.5 mol?L-1氯化钙溶液中Cl-浓度为3mol/L,与50mL1mol/L的AlCl3溶液中的Cl-浓度相等,故B不选;
C、150mL 3 mol?L-1氯化钾溶液中Cl-浓度为6mol/L,与50mL1mol/L的AlCl3溶液中的Cl-浓度不相等,故C不选;
D、75mL 1 mol?L-1氯化铁溶液中Cl-浓度为2mol/L,与50mL1mol/L的AlCl3溶液中的Cl-浓度不相等,故D不选.
故选:A.
A、150ml1mol/L的NaCl溶液中Cl-浓度为1mol/L,与50mL1mol/L的AlCl3溶液中的Cl-浓度不相等,故A选;
B、75mL 1.5 mol?L-1氯化钙溶液中Cl-浓度为3mol/L,与50mL1mol/L的AlCl3溶液中的Cl-浓度相等,故B不选;
C、150mL 3 mol?L-1氯化钾溶液中Cl-浓度为6mol/L,与50mL1mol/L的AlCl3溶液中的Cl-浓度不相等,故C不选;
D、75mL 1 mol?L-1氯化铁溶液中Cl-浓度为2mol/L,与50mL1mol/L的AlCl3溶液中的Cl-浓度不相等,故D不选.
故选:A.
点评:本题考查物质的量浓度的计算与理解,题目难度不大,注意溶液中溶质离子的浓度与溶液体积无关,只取决于物质电离出的离子的数目多少与溶质的浓度.

练习册系列答案
相关题目
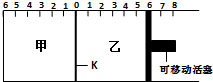 如图所示,甲、乙之间的隔板K可以左右移动,甲中充入2molA和1molB,乙中充入2molC和1molHe,此时K停在0处.在一定条件下发生可逆反应:2A(g)+B(g)?2C(g),反应达到平衡后,恢复到反应发生前的温度.下列有关说法正确的是( )
如图所示,甲、乙之间的隔板K可以左右移动,甲中充入2molA和1molB,乙中充入2molC和1molHe,此时K停在0处.在一定条件下发生可逆反应:2A(g)+B(g)?2C(g),反应达到平衡后,恢复到反应发生前的温度.下列有关说法正确的是( )| A、根据隔板K滑动与否不能判断左右两边的反应是否达到平衡 |
| B、若平衡时K停留在左侧1处,则活塞仍停留在右侧6处 |
| C、到达平衡时,甲容器中C的物质的量等于乙容器中C的物质的量 |
| D、达到平衡后,隔板K最终停留在左侧刻度0--2之间 |
金属冶炼一般有下列四种方法:①焦炭法 ②水煤气(或H2、CO)法 ③活泼金属置换法④电解法.这四种方法在工业上均有应用.古代有:(Ⅰ)火烧孔雀石炼铜;(Ⅱ)湿法炼铜.现代有:(Ⅲ)铝热法炼铬;(Ⅳ)从光卤石中炼镁.对它们的冶炼方法的分析,不正确的是( )
| A、(Ⅰ),① |
| B、(Ⅱ),② |
| C、(Ⅲ),③ |
| D、(Ⅳ),④ |
下列说法中正确的是( )
| A、在Na3PO4溶液中,c(Na+) 是c(PO43-)的3倍 |
| B、pH=1的盐酸中,其c(H+)是pH=3的盐酸的1000倍 |
| C、0.1mol/L KOH溶液和0.1mol/L氨水中,其c(OH-)相等 |
| D、无论是酸性、碱性还是中性溶液中,其c(H+)和c(OH-)的乘积都等于1×10-14 |
H+(aq)+OH-(aq)=H2O(l)△H=a,则a可能等于( )
| A、-57.3mol/L |
| B、-57.3kJ/mol |
| C、+57.3J/mol |
| D、-57.3J/mol |
如图所示是298K时,N2与H2反应过程中能量变化的曲线图,下列叙述正确的是( )


| A、该反应的热化学方程式为:N2+3H2?2NH3△H=-92 kJ/mol |
| B、b曲线是加入催化剂时的能量变化曲线 |
| C、加入催化剂,该化学反应的反应热改变 |
| D、升高温度,正、逆反应速率都增大,平衡向逆方向移动 |
如图两瓶体积相等的气体,在同温、同压时瓶内气体的关系一定正确的是( ) 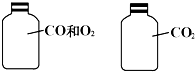
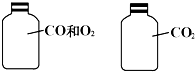
| A、所含原子数相等 |
| B、所含分子数相等 |
| C、气体质量相等 |
| D、所含C原子数相等 |