题目内容
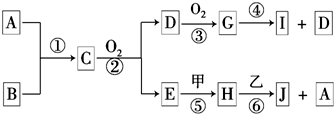
已知:A、B为常见的非金属单质且均为气体;甲、乙为金属单质,乙在I的浓溶液中发生钝化;C、H、J的溶液均呈碱性.各物质间的转化关系如下(部分生成物未给出,且未注明反应条件):
(1)写出反应②的化学方程式为 .
(2)反应④中每消耗1mol G,转移电子的物质的量为 .
(3)反应⑥的离子方程式是 .
(4)实验室中保存I的方法是 .原因是 用化学方程式表示)

(1)写出反应②的化学方程式为
(2)反应④中每消耗1mol G,转移电子的物质的量为
(3)反应⑥的离子方程式是
(4)实验室中保存I的方法是
考点:无机物的推断
专题:推断题
分析:A、B为常见的非金属单质且均为气体;甲、乙为金属单质,乙在I的浓溶液中发生钝化;C、H、J的溶液均呈碱性,则C为NH3,D为NO,G为NO2,反应④为G与水的反应,I为硝酸;结合转化及溶液的碱性,则甲为Na,E为水,H为NaOH,乙为Al,反应⑥为Al与NaOH溶液反应,则J为NaAlO2,A为H2,所以B为氮气,然后结合物质的性质及题目要求来解答.
解答:
解:A、B为常见的非金属单质且均为气体;甲、乙为金属单质,乙在I的浓溶液中发生钝化;C、H、J的溶液均呈碱性,则C为NH3,D为NO,G为NO2,反应④为G与水的反应,I为硝酸;结合转化及溶液的碱性,则甲为Na,E为水,H为NaOH,乙为Al,反应⑥为Al与NaOH溶液反应,则J为NaAlO2,A为H2,所以B为氮气,
(1)反应②的化学方程式为4NH3+5O2
4NO+6H2O,故答案为:4NH3+5O2
4NO+6H2O;
(2)由3NO2+H2O═HNO3+NO可知,3molG参加反应转移2mol电子,则每消耗1molG,转移电子的物质的量为
mol=0.67mol,
故答案为:0.67mol;
(3)反应⑥的离子方程式为2Al+2H2O+2OH-═2AlO2-+3H2↑,故答案为:2Al+2H2O+2OH-═2AlO2-+3H2↑;
(4)I为硝酸,见光易分解,则保存在棕色试剂瓶中,放在阴凉处,因为硝酸加热或见光分解,反应的化学方程式为:4HNO3
4NO2↑+O2+2H2O
;
故答案为:保存在棕色试剂瓶中,放在阴凉处,4HNO3
4NO2↑+O2+2H2O;
(1)反应②的化学方程式为4NH3+5O2
| ||
| △ |
| ||
| △ |
(2)由3NO2+H2O═HNO3+NO可知,3molG参加反应转移2mol电子,则每消耗1molG,转移电子的物质的量为
| 2 |
| 3 |
故答案为:0.67mol;
(3)反应⑥的离子方程式为2Al+2H2O+2OH-═2AlO2-+3H2↑,故答案为:2Al+2H2O+2OH-═2AlO2-+3H2↑;
(4)I为硝酸,见光易分解,则保存在棕色试剂瓶中,放在阴凉处,因为硝酸加热或见光分解,反应的化学方程式为:4HNO3
| ||
;
故答案为:保存在棕色试剂瓶中,放在阴凉处,4HNO3
| ||
点评:本题考查无机物的推断,注意钝化及溶液的碱性来推断各物质是解答的关键,C为氨气是解答本题的突破口,题目难度中等.

练习册系列答案
相关题目
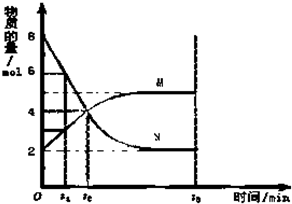 在一定温度下,在容积为2L的容器内,某反应各物质(均为气体)的物质的量随反应时间的变化曲线如图,试回答下列问题:
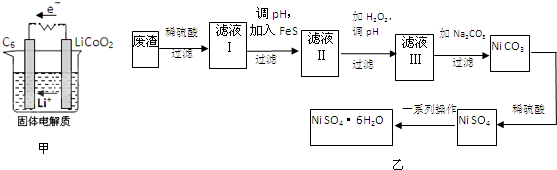
在一定温度下,在容积为2L的容器内,某反应各物质(均为气体)的物质的量随反应时间的变化曲线如图,试回答下列问题: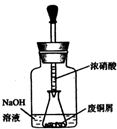 碱式碳酸铜 Cu2(OH)2CO3是一种用途广泛的化工原料,实验室以废铜屑为原料制取碱式碳酸铜的步骤如下:
碱式碳酸铜 Cu2(OH)2CO3是一种用途广泛的化工原料,实验室以废铜屑为原料制取碱式碳酸铜的步骤如下: