题目内容
(8分) CH3OH(g)+H2O(g) CO2(g)+3H2(g);该反应的正反应为吸热反应,请根据题目要求回答下列问题:
CO2(g)+3H2(g);该反应的正反应为吸热反应,请根据题目要求回答下列问题:
(1)在其它条件不变的情况下降低温度,则逆反应速率 (填“增大”或“减小”或“不变”,下同);在其它条件不变的情况下加压,则正反应速率 。
(2)一定条件下,向体积为2L的密闭容器中充入1molCH3OH(g)和3molH2O(g),20s 后,测得混合气体的压强是反应前的1.2倍,则用甲醇表示该反应的速率为 。
(3)判断该可逆反应达到平衡状态的依据是(填序号) 。
A v正(CH3OH)=v正(CO2)
B 混合气体的密度不变
C 混合气体的平均相对分子质量不变
D CH3OH、H2O、CO2、H2的浓度都不再发生变化
(4)在一定条件下,当该反应处于化学平衡状态时,下列操作可使化学平衡向逆反应方 向移动的是 (填序号)。
A.升高温度 B.降低温度 C.增大压强
(1)减小;增大 (2)0.01mol/(L·s)(3)CD (4)BC
解析

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
| 在温度相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒压,测得反应达到平衡时的有关数据如表 (已知CO(g)+2H2(g)  CH3OH(g)△H=-90.7kJ/mol) CH3OH(g)△H=-90.7kJ/mol)
|
 将CO2转化成甲醇燃料是减排,环保的一种科学方法,其原理
将CO2转化成甲醇燃料是减排,环保的一种科学方法,其原理为:CO2(g)+3H2(g)
| 一定条件 |
△H<0500℃时,在体积为lL的固定容积密闭容器中充人
lmol CO2,3mol H2,测得CO2浓度与甲醇浓度随时间变
化如图所示;从中得出下列结论中错误的( )
| A、曲线x表示可以CH3OH浓度变化,曲线Y表示CO2浓度变化 |
| B、从反应开始到平衡,氢气的反应速率v(H2)=0.225mol/(L?min) |
| C、平衡时H2的转化率为75% |
| D、该反应的平衡常数K=3 |
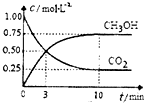 已知:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.OkJ?mol-1 一定条件下,向体积为11的密闭容器中充入lmolCO2和3mol H2,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示.下列叙述中正确的是( )
已知:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.OkJ?mol-1 一定条件下,向体积为11的密闭容器中充入lmolCO2和3mol H2,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示.下列叙述中正确的是( )| A、升高温度平衡常数K增大 | B、反应达到平衡状态时,CO2的平衡转化率为75% | C、3min时,用CO2的浓度表示的正反应速率等于用CH3OH的浓度表示的逆反应速率 | D、从反应开始到平衡,H2的平均反应速率v (H2)=0.075mol?L-1?min-1 |

 煤直接燃烧的能量利用率较低,为提高其利用率,工业上将煤气化(转变成CO和H2)后再合成乙醇、二甲醚等多种能源.
煤直接燃烧的能量利用率较低,为提高其利用率,工业上将煤气化(转变成CO和H2)后再合成乙醇、二甲醚等多种能源.