题目内容
下列叙述I和II均正确且具有因果关系的是( )
| 编号 | 叙述I | 叙述II |
| A | 金属活动性铜比铁弱 | 镀铜铁制品表层划损后仍然受到保护 |
| B | 金属钠有还原性 | 用金属钠检验无水乙醇中是否含有少量水 |
| C | Ksp(CaCO3)<Ksp(CaSO4) | 用Na2CO3溶液和盐酸除水垢CaSO4 |
| D | Cl2具有漂白性 | 用氯气制盐酸 |
| A、A | B、B | C、C | D、D |
考点:金属的电化学腐蚀与防护,难溶电解质的溶解平衡及沉淀转化的本质,氯气的化学性质,钠的化学性质
专题:
分析:A、镀铜铁制品表层划损后形成原电池,金属铁是负极,被腐蚀;
B、金属钠和乙醇均可以和水反应产生氢气;
C、沉淀向着Ksp更小的方向转化;
D、氯气不具有漂白性.
B、金属钠和乙醇均可以和水反应产生氢气;
C、沉淀向着Ksp更小的方向转化;
D、氯气不具有漂白性.
解答:
解:A、镀铜铁制品表层划损后形成原电池,金属铁是负极,被腐蚀,所以叙述II是错误的,故A错误;
B、金属钠和乙醇均可以和水反应产生氢气,所以无法用金属钠检验无水乙醇中是否含有少量水,叙述II是错误的,故B错误;
C、沉淀向着Ksp更小的方向转化,向硫酸钙中碳酸钠,会发生反应转化为碳酸钙,在加入盐酸,可以和碳酸钙反应,得到易溶于水的氯化钙溶液,故C正确;
D、氯气不具有漂白性,所以叙述I是错误的,故D错误;
故选C.
B、金属钠和乙醇均可以和水反应产生氢气,所以无法用金属钠检验无水乙醇中是否含有少量水,叙述II是错误的,故B错误;
C、沉淀向着Ksp更小的方向转化,向硫酸钙中碳酸钠,会发生反应转化为碳酸钙,在加入盐酸,可以和碳酸钙反应,得到易溶于水的氯化钙溶液,故C正确;
D、氯气不具有漂白性,所以叙述I是错误的,故D错误;
故选C.
点评:本题涉及金属的腐蚀和防护、沉淀的转化以及物质的性质等知识,注意知识的归纳和梳理是解题的关键,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Fe2+、Al3+和Na+某同学为了确认其成分,取部分试液,设计并完成了如下实验:由此可知原溶液中( )


| A、原溶液中c(Fe3+)=0.2mol?L-1 |
| B、要确定原溶液中是否含有Fe2+,其操作为:取少量原溶液于试管中,加入适量氨水,在加KSCN溶液,溶液呈血红色,则含有Fe2+ |
| C、SO42-、NH4+、Na+一定,CO32-、Al3+一定不存在 |
| D、溶液中至少有4种离子存在,其中Cl-一定存在,且c(Cl-)≥0.2mol?L -1 |
下列说法中正确的是( )
| A、用乙醇从碘水中萃取碘 |
| B、真假羊毛线可以通过灼烧的方法进行鉴别 |
| C、八宝粥(含桂圆、红豆、糯米等)不加糖,比加糖还甜,糖尿病人可以放心食用 |
D、 和 和 是同系物 是同系物 |
将Na2CO3?10H2O和NaHCO3、Na2CO3组成的混合物10.68g,溶于水制成100ml溶液,其中Na+的浓度为1.4mol/L,若将等质量的该混合物加热到恒重,计算所得固体的质量为多少?
下列各组物质之间,一定是互为同系物的是( )
| A、HCHO与HCOOCH3 |
| B、HOCH2CH3与CH3COOH |
| C、HCOOH与C17H35COOH |
| D、C2H4与C3H6 |
化学与社会、生活密切相关.下列说法正确的是( )
| A、SO2可用作漂白剂是因为其具有氧化性 |
| B、半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是二氧化硅 |
| C、洁厕灵(有效成分为HCl)与84消毒液(有效成分为NaClO)混合使用可增加卫浴的清洁效果 |
| D、高铁酸钾(K2FeO4)是一种高效、多功能水处理剂,既能消毒杀菌又能净水 |


 )和乳酸(
)和乳酸( )为有机物原料合成化工原料肉桂酸(
)为有机物原料合成化工原料肉桂酸(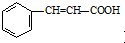 ),涉及的反应方程式为
),涉及的反应方程式为