题目内容
下列说法正确的是( )
| A、需要加热的化学反应都不能自发进行 |
| B、中和反应都是放热反应 |
| C、原电池是将电能转化为化学能的装置 |
| D、太阳能电池可将化学能转化为电能 |
考点:吸热反应和放热反应,常见的能量转化形式
专题:
分析:A、化学反应进行的方向由△G=△H-T△S决定,△G<0就可以自发进行;
B、中和反应为放热反应;
C、原电池是将化学能转化为电能的一种装置;
D、太阳能电池是将太阳能转化为电能的装置.
B、中和反应为放热反应;
C、原电池是将化学能转化为电能的一种装置;
D、太阳能电池是将太阳能转化为电能的装置.
解答:
解:A.化学反应进行的方向由△G=△H-T△S决定,△G<0就可以自发进行,故A错误;
B.中和反应为放热反应,故B正确;
C.原电池是将化学能转化为电能的一种装置,故C错误;
D.太阳能电池是将太阳能转化为电能的装置,故D错误.
故选B.
B.中和反应为放热反应,故B正确;
C.原电池是将化学能转化为电能的一种装置,故C错误;
D.太阳能电池是将太阳能转化为电能的装置,故D错误.
故选B.
点评:本题考查较为综合,侧重于化学反应与能量的变化,为高考常见题型,难度不大,注意相关基础知识的积累.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
已知Kφ(AgCl)=1.8×10-10mol2?L-2,Kφ(AgBr)=5.0×10-13mol2?L-2,Kφ(Ag2CrO4)=9.0×10-12mol2?L-3.某溶液中含有Cl-、Br-和CrO42-,浓度均为0.10mol?L-1,向该溶液中逐滴加入0.10mol?L-1的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为( )
| A、Cl-、Br-、CrO42- |
| B、CrO42-、Br-、Cl- |
| C、Br-、Cl-、CrO42- |
| D、Br-、CrO42-、Cl- |
某温度下,浓度都为1mol/L的两种气体X2和Y2,在密闭容器中反应生成气体Z.反应2min后,测得 X2的浓度为0.4mol/L,用Y2的变化表示的反应速率v(Y2)=0.1mol/(L?min),生成的c(Z)=0.4mol/L,如z用X、Y表示,则该反应方程式是( )
| A、X2+2Y2═2XY2 |
| B、2X2+Y2═2X2Y |
| C、3X2+Y2═2X3Y |
| D、X2+3Y2═2XY3 |
已知反应:①101kPa时,2C(s)+O2(g)=2CO(g)△H=-221kJ/mol
②稀溶液中,H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol 下列结论正确的是( )
②稀溶液中,H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol 下列结论正确的是( )
| A、反应①的反应热为221kJ |
| B、碳的燃烧热为△H=-221kJ/mol |
| C、稀硫酸与稀NaOH溶液反应的中和热为△H=-57.3kJ/mol |
| D、稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量 |
向足量H2SO4溶液中加入100mL 0.4mol?L-1 Ba(OH)2溶液,放出的热量是5.12kJ.如果向足量Ba(OH)2溶液中加入100mL 0.4mol?L-1盐酸时,放出的热量为2.2 kJ.则Na2SO4溶液与BaCl2溶液反应的热化学方程式为( )
| A、Ba2+(aq)+SO42-(aq)═BaSO4(s)△H=-2.92 kJ?mol-1 |
| B、Ba2+(aq)+SO42-(aq)═BaSO4(s)△H=-18 kJ?mol-1 |
| C、Ba2+(aq)+SO42-(aq)═BaSO4(s)△H=-73 kJ?mol-1 |
| D、Ba2+(aq)+SO42-(aq)═BaSO4(s)△H=-0.72 kJ?mol-1 |
已知下列氧化还原反应:2BrO3-+Cl2═Br2+2ClO3-,5Cl2+I2+6H2O═2IO3-+10Cl-+12H+,ClO3-+5Cl-+6H+═3Cl2↑+3H2O.上述条件下,各微粒氧化性由强到弱的排列顺序正确的是( )
| A、ClO3->BrO3->IO3->Cl2 |
| B、BrO3->Cl2>ClO3->IO3- |
| C、BrO3->ClO3->Cl2>IO3- |
| D、Cl2>BrO3->ClO3->IO3- |
下列反应,1)符合图象描述特点,2)对其进行分析,结论是正确的.则合理选项为( )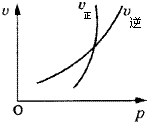

| A、N2O3(g)?NO2(g)+NO(g); 恒容时加入N2O3,平衡正向移动 |
| B、N2(g)+3H2(g)?2NH3(g); 将氨气液化分离后,有利于加快正反应速率 |
| C、4NH3(g)+5O2(g)?4NO(g)+6H2O(g); 加大氧气浓度,能提高氨气平衡转化率 |
| D、2SO2(g)+O2(g)?2SO3(g); 增大压强,平衡常数不变 |