题目内容
氮化钠(Na3N)是科学家制备的一种重要的化合物,它与水作用可产生NH3,请回答下列问题:
(1)Na3N的电子式 ,该化合物是由 键形成的.
(2)Na3N与盐酸反应生成 种盐.
(3)Na3N与水的反应属于 反应.
(1)Na3N的电子式
(2)Na3N与盐酸反应生成
(3)Na3N与水的反应属于
考点:钠的重要化合物
专题:元素及其化合物
分析:氮化钠为离子化合物,可与盐酸反应生成氯化钠和氯化铵,与水反应生成氢氧化钠和氨气,以此解答该题.
解答:
解:(1)钠元素和氮元素分别是活泼的金属和活泼的非金属,所以二者形成的化学键是离子键,Na3N的电子式为: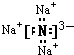 ,
,
故答案为: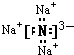 ;离子;
;离子;
(2)氮化钠和水反应生成氨气和氢氧化钠,Na3N+3H2O=NH3+3NaOH,
氨气和盐酸反应生成氯化铵:NH3+HCl=NH4Cl,
氢氧化钠和盐酸反应生成氯化钠和水:NaOH+HCl=NaCl+H2O,
根据反应方程式知,生成的盐有:NaCl、NH4Cl,所以生成两种盐,
故答案为:2;
(3)氮化钠和水发生了复分解反应,反应的方程式是:Na3N+3H2O=3NaOH+NH3↑,
故答案为:复分解.
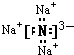 ,
,故答案为:
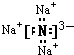 ;离子;
;离子;(2)氮化钠和水反应生成氨气和氢氧化钠,Na3N+3H2O=NH3+3NaOH,
氨气和盐酸反应生成氯化铵:NH3+HCl=NH4Cl,
氢氧化钠和盐酸反应生成氯化钠和水:NaOH+HCl=NaCl+H2O,
根据反应方程式知,生成的盐有:NaCl、NH4Cl,所以生成两种盐,
故答案为:2;
(3)氮化钠和水发生了复分解反应,反应的方程式是:Na3N+3H2O=3NaOH+NH3↑,
故答案为:复分解.
点评:本题考查钠的化合物,为高频考点,侧重于基础性试题的考查,试题基础性强,注重能力的考查,该题有利于巩固学生对教材基础知识的理解,培养学生的规范答题能力,提高学习效率,难度不大.

练习册系列答案
相关题目
下列叙述不正确的是( )
| A、水晶和玛瑙的主要成分都是SiO2 |
| B、钢是目前用量最大的合金 |
| C、金属铝的熔点很高,可用作耐火材料 |
| D、单质硅可用作太阳能电池的材料 |
下列分散系属于胶体的是( )
| A、淀粉溶液 | B、食盐水 |
| C、牛奶 | D、碘酒 |