题目内容
4.下列粒子(或化学键)的数目之比不是1:1的是( )| A. | 氘原子(12H)中的质子和中子 | B. | CsCl晶胞中的Cs+和Cl- | ||
| C. | Na2O2固体中的阴离子和阳离子 | D. | CO2分子中的σ键和π键 |
分析 A.氘原子(12H)中质子数为1,中子数为2-1=1;
B.CsCl为离子晶体,由化学式可知,阴阳离子个数比为1:1;
C.Na2O2中阳离子为钠离子,阴离子为过氧根离子;
D.CO2分子结构为O=C=O,双键中含1个σ键、1个π键.
解答 解:A.氘原子(12H)中质子数为1,中子数为2-1=1,则质子和中子的数目之比是1:1,故A不选;
B.CsCl为离子晶体,由化学式可知,阴阳离子个数比为1:1,则Cs+和Cl-的数目之比是1:1,故B不选;
C.Na2O2中阳离子为钠离子,阴离子为过氧根离子,则阴离子和阳离子的数目之比是1:2,故C选;
D.CO2分子结构为O=C=O,双键中含1个σ键、1个π键,则σ键和π键的数目之比是1:1,故D不选;
故选C.
点评 本题考查化学键,为高频考点,把握化学键的判断、物质构成微粒为解答的关键,侧重分析与应用能力的考查,注意物质的构成及应用,题目难度不大.

练习册系列答案
 寒假学与练系列答案
寒假学与练系列答案
相关题目
14.化学科学需要借助化学专用语言来描述,下列有关化学用语正确的是( )
| A. | 质量数为37的氯原子:$\stackrel{17}{37}$Cl | B. | H2O的结构式:H-O-H | ||
| C. | CH4分子的比例模型: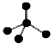 | D. | 氯化铵的电子式: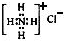 |
12.下列叙述错误的是( )
| A. | 蚕丝、羊毛、棉花的主要成分都是蛋白质 | |
| B. | 纤维素、油脂、蛋白质都能水解,但水解产物不同 | |
| C. | 油脂在碱的催化作用下可发生水解,工业上利用该反应生产肥皂 | |
| D. | 乙酸乙酯中的少量乙酸可用饱和Na2CO3溶液除去 |
19. NPG(新戊二醇)是一种可用作太阳能储存热量的物质.已知:NPG的结构式如图.有关NPG的说法不正确的是( )
NPG(新戊二醇)是一种可用作太阳能储存热量的物质.已知:NPG的结构式如图.有关NPG的说法不正确的是( )
 NPG(新戊二醇)是一种可用作太阳能储存热量的物质.已知:NPG的结构式如图.有关NPG的说法不正确的是( )
NPG(新戊二醇)是一种可用作太阳能储存热量的物质.已知:NPG的结构式如图.有关NPG的说法不正确的是( )| A. | NPG的分子式为C5H12O2 | B. | NPG沸点比乙二醇的高 | ||
| C. | NPG一定条件下能发生消去反应 | D. | NPG的氧化产物可发生银镜反应 |
9.下列说法中正确的是( )
| A. | 石油的分馏和煤的干馏都是物理变化 | |
| B. | 油脂、淀粉、纤维素都是高分子化合物 | |
| C. | 酯类物质是形成水果香味的主要成分 | |
| D. | 纤维素和淀粉互为同分异构体 |
13.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 1molSiO2含NASiO2个分子 | |
| B. | 12g金刚石晶体中碳碳单键的数目为2NA | |
| C. | 1L0.1mol/LFeCl3溶液中含Fe3+的数目为0.1NA | |
| D. | 一定条件下,1molN2和3molH2完全反应,电子转移的数目为6NA |

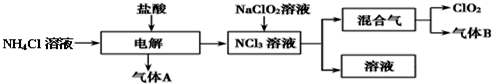
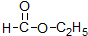 酯; ②
酯; ②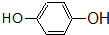 酚;
酚;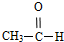 醛;④
醛;④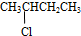 卤代烃;⑤
卤代烃;⑤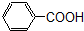 羧酸;
羧酸;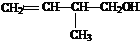
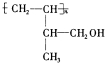 .
.