题目内容
盛满NO2的试管倒置于水槽中,反应完毕后,液面上升的高度是试管的( )
A、
| ||
B、
| ||
C、
| ||
D、
|
考点:氮的氧化物的性质及其对环境的影响
专题:元素及其化合物
分析:依据二氧化氮和水反应生成一氧化氮和一氧化氮的定量关系分析计算.
解答:
解:盛满NO2的试管倒置于水槽中,反应完毕后,3NO2+H2O=2HNO3+NO,液面上升的高度是试管的
,
故选C.
| 2 |
| 3 |
故选C.
点评:本题考查了化学方程式定量关系的分析计算,注意反应前后气体体积变化的特征,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
下列排列顺序正确的是( )
①固体的热稳定性:CaCO3>Na2CO3>NaHCO3;
②还原性:SO32->I->Br-;
③微粒半径:K+>Na+>O2-;
④结合H+的能力:OH->AlO2->HCO3-;
⑤氢化物的沸点:H2O>NH3>HF.
①固体的热稳定性:CaCO3>Na2CO3>NaHCO3;
②还原性:SO32->I->Br-;
③微粒半径:K+>Na+>O2-;
④结合H+的能力:OH->AlO2->HCO3-;
⑤氢化物的沸点:H2O>NH3>HF.
| A、①③ | B、②④ | C、①② | D、③⑤ |
下列事实不能用勒夏特列原理解释的是( )
| A、溴水中有下列平衡Br2+H2O?HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅 |
| B、已知,N2(g)+3 H2(g)?2NH3(g)△H<0,为提高氨的产率,理论上应采取降低温度的措施 |
| C、反应CO(g)+NO2(g)?CO2(g)+NO(g)△H<0,达平衡后,升高温度体系颜色变深 |
| D、对于2HI(g)?H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深 |
下列说法中,正确的是( )
| A、通常状况下,N2和H2、O2都能反应 |
| B、在实验室收集NO气体可用排气法 |
| C、一定条件下,白磷转变成红磷是物理变化 |
| D、NO2是造成光化学烟雾污染的主要因素 |
已知1g氢气完全燃烧生成水蒸气时放出热量121kJ,且氢气中1mol H-H 键完全断裂时吸收热量436kJ,水蒸气中1mol H-O 键形成时放出热量463kJ,则氧气中1mol O=O 键断裂时吸收热量为( )
| A、188kJ |
| B、248 kJ |
| C、124kJ |
| D、496kJ |
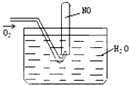 如图进行实验,试管内装有12mL NO,然后间歇而缓慢地通入8mL O2.下面有关实验最终状态的描述正确的是( )
如图进行实验,试管内装有12mL NO,然后间歇而缓慢地通入8mL O2.下面有关实验最终状态的描述正确的是( )| A、试管内气体呈棕红色 |
| B、试管内气体为无色的NO |
| C、试管内气体为无色的O2 |
| D、试管内液面高度上升到试管底部 |
下列离子方程式正确的是( )
| A、等体积等物质的量浓度的NaHCO3和Ba(OH)2两溶液混合:2HCO3-+Ba2++2OH-=BaCO3↓+H2O+CO32- | ||||
| B、Na2S溶液吸收足量SO2:S2-+2SO2+2 H2O=2HSO3-+H2S↑ | ||||
| C、硫酸氢镁溶液中加入足量氢氧化钠:Mg2++2OHˉ=Mg(OH)2↓ | ||||
D、用铜为电极电解稀硫酸溶液:Cu+2H+
|
下列说法中不正确的是( )
| A、按系统命名法:CH3CH2C(CH3)2CH(C2H5)CH3的正确名称是3,3,4-三甲基己烷 |
| B、所有的糖、油脂、蛋白质都能水解,但水解产物不同 |
C、1mol的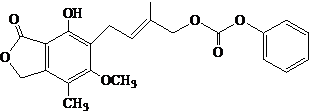 最多能与含5mol NaOH的水溶液完全反应 最多能与含5mol NaOH的水溶液完全反应 |
D、若完全燃烧,1mol雄酮( 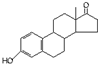 )比雌酮( )比雌酮(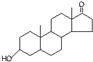 )多消耗3mol O2. )多消耗3mol O2. |
上世纪80年代后期,人们发现NO在人体内起着多方面重要的生理作用.下列关于NO的说法错误的是( )
| A、NO是汽车尾气的有害成分之一 |
| B、NO是具有刺激性气味的红棕色气体 |
| C、NO极少量时在人体的血管系统内会促进血管扩张,防止血管栓塞 |
| D、NO能够与人体血红蛋白结合,吸入较多会造成人体缺氧中毒 |