题目内容
15.下列装置或操作正确的是( )| A. | 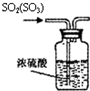 净化SO2 | B. | 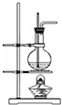 制硝基苯 | C. |  银镜反应 | D. | 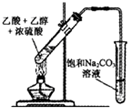 制取乙酸乙酯 |
分析 A.浓硫酸可吸收三氧化硫,与二氧化硫不反应;
B.制备硝基苯,需要水浴加热;
C.银镜反应需要水浴加热;
D.导管在碳酸钠溶液的液面下,可发生倒吸.
解答 解:A.浓硫酸可吸收三氧化硫,与二氧化硫不反应,则图中导管长进短出可净化SO2,故A正确;
B.制备硝基苯,需要水浴加热,控制水浴温度为50~60℃,故B错误;
C.银镜反应需要水浴加热,图中为直接加热,操作不合理,故C错误;
D.导管在碳酸钠溶液的液面下,可发生倒吸,导管口应在液面上,故D错误;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,把握混合物分离提纯、有机物的制备及性质实验、实验装置的作用为解答的关键,侧重分析与实验能力的考查,注意实验技能及实验评价性分析,题目难度不大.

练习册系列答案
相关题目
5.某原电池总反应的离子方程式为Cu2++Fe=Fe2++Cu能实现该反应的原电池组成是( )
| A. | 正极为铁,负极为铁,电解质溶液为CuCl2溶液 | |
| B. | 正极为银,负极为铁,电解质液为Fe(NO3)3溶液 | |
| C. | 正极为碳,负极为锌,电解质溶液为Fe2(SO4)3溶液 | |
| D. | 正极为碳,负极为铁,电解质溶液为CuSO4溶液 |
10.下列离子方程式正确的是( )
| A. | 石灰乳与碳酸钠溶液混合:Ca2++CO32-→CaCO3↓ | |
| B. | 向Ba(OH)2溶液中逐滴加入NH4HSO4 溶液,刚好沉淀完全:Ba2++2OH-+2H++SO42-→BaSO4↓+2H2O | |
| C. | 向亚硫酸钡固体中加入稀硝酸:3BaSO3+2H++2NO3-→3BaSO4↓+2NO↑+H2O | |
| D. | 碳酸氢钠溶液中加入过量的氢氧化钙溶液:2HCO3-+Ca2++2OH-→CaCO3↓+2H2O+CO32- |
20.一定量饱和Na2CO3溶液中逐滴加入稀盐酸直至过量,开始阶段无现象,后来冒气泡.以下判断错误的是( )
| A. | CO32-离子是弱酸根,开始阶段与H+结合,生成HCO3- | |
| B. | 溶液中的Na+、Cl-抑制了CO2生成 | |
| C. | 开始生成的CO2与Na2CO3反应,生成了NaHCO3 | |
| D. | CO32-离子在水中,存在两个水解平衡,开始阶段可能是H+结合OH-,生成HCO3- |
7.下列混和物可用分液漏斗分离的是( )
| A. | 苯和植物油 | B. | 乙酸乙酯与饱和碳酸钠溶液 | ||
| C. | 甘油和水 | D. | 苯和液溴 |
4.将物质的量共为amol的NaNO3、Cu(NO3)2和AgNO3的固体混合物用酒精灯加热至恒重,收集到的气体再用足量的水吸收,剩余气体为bmol,则b不可能为( )
| A. | 0.25a | B. | 0.35a | C. | 0.45a | D. | 0.50a |
5.如图是三种常见有机物的比例模型示意图.下列说法正确的是( )

| A. | 甲在光照条件下与Cl2反应可得到四种不同的产物 | |
| B. | 乙、丙所有的原子均处于同一平面,均可使溴水反应褪色 | |
| C. | 石油分馏可获得甲和乙,煤干馏可获得丙 | |
| D. | 在浓硫酸存在下,丙与浓硝酸共热的反应属于取代反应 |
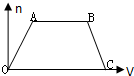 将足量CO2通入NaOH和Ba(OH)2的混合稀溶液中,生成沉淀的物质的量(n)和通入CO2气体的体积(V)的关系如图所示,图中AB段表示的离子方程式先后顺序正确的是( )
将足量CO2通入NaOH和Ba(OH)2的混合稀溶液中,生成沉淀的物质的量(n)和通入CO2气体的体积(V)的关系如图所示,图中AB段表示的离子方程式先后顺序正确的是( )