题目内容
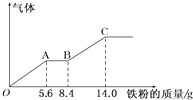 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解9.6g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体).下列分析或结果正确的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解9.6g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体).下列分析或结果正确的是( )| A、原混合酸中HNO3的物质的量为0.1 mol |
| B、OA段产生的是氢气,BC段产生NO |
| C、AB段的反应为Fe+2Fe(NO3)3═3 Fe(NO3)2 |
| D、H2SO4浓度为2.5 mol?L-1 |
考点:化学方程式的有关计算,有关混合物反应的计算
专题:计算题
分析:由图象可知,由于铁过量,OA段发生反应为:Fe+NO3-+4H+=Fe3++NO↑+2H2O,AB段发生反应为:Fe+2Fe3+=3Fe2+,BC段发生反应为:Fe+2H+=Fe2++H2↑;
A.OA段发生反应为:Fe+NO3-+4H+=Fe3++NO↑+2H2O,硝酸全部起氧化剂作用,根据铁的物质的量结合离子方程式计算;
B.OA段产生NO,BC段生成氢气;
C.OA段中硝酸根全部被还原,AB段为Fe与硫酸铁反应生成硫酸亚铁;
D.加入Fe粉14gL时,完全反应,此时溶液中溶质为FeSO4,根据守恒可知n(FeSO4)=n(H2SO4),进而确定硫酸的浓度.
A.OA段发生反应为:Fe+NO3-+4H+=Fe3++NO↑+2H2O,硝酸全部起氧化剂作用,根据铁的物质的量结合离子方程式计算;
B.OA段产生NO,BC段生成氢气;
C.OA段中硝酸根全部被还原,AB段为Fe与硫酸铁反应生成硫酸亚铁;
D.加入Fe粉14gL时,完全反应,此时溶液中溶质为FeSO4,根据守恒可知n(FeSO4)=n(H2SO4),进而确定硫酸的浓度.
解答:
解:A.OA段发生反应为:Fe+NO3-+4H+=Fe3++NO↑+2H2O,硝酸全部起氧化剂作用,每份溶液中n(NO3-)=n(Fe),所以原混合酸中n(HNO3)=2n(Fe)=2×
=0.2mol,故A错误;
B.由图象可知,由于铁过量,OA段发生反应为:Fe+NO3-+4H+=Fe3++NO↑+2H2O,AB段发生反应为:Fe+2Fe3+=3Fe2+,BC段发生反应为:Fe+2H+=Fe2++H2↑,故B错误;
C.OA段中硝酸根全部被还原,AB段为Fe与硫酸铁反应生成硫酸亚铁,反应为Fe+Fe2(SO4)3═3 FeSO4,故C错误;
D.加入Fe粉14时,完全反应,此时溶液中溶质为FeSO4,反应消耗铁的物质的量=
=0.25mol,根据守恒可知n(H2SO4)=n(FeSO4)=n(Fe)=0.25mol,所以硫酸的浓度是
=2.5mol/L,故D正确,
故选D.
| 5.6g |
| 56g/mol |
B.由图象可知,由于铁过量,OA段发生反应为:Fe+NO3-+4H+=Fe3++NO↑+2H2O,AB段发生反应为:Fe+2Fe3+=3Fe2+,BC段发生反应为:Fe+2H+=Fe2++H2↑,故B错误;
C.OA段中硝酸根全部被还原,AB段为Fe与硫酸铁反应生成硫酸亚铁,反应为Fe+Fe2(SO4)3═3 FeSO4,故C错误;
D.加入Fe粉14时,完全反应,此时溶液中溶质为FeSO4,反应消耗铁的物质的量=
| 14g |
| 56g/mol |
| 0.25mol |
| 0.1L |
故选D.
点评:本题以化学反应图象为载体,考查有关金属和酸反应的计算,难度中等,关键根据图象分析各段发生的反应,注意与铁的反应中硝酸全部起氧化剂作用,A选项为易错点,学生容易按每一份计算解答.

练习册系列答案
相关题目
根据中学化学教材所附元素周期表判断,下列叙述正确的是( )
| A、M电子层电子数为奇数的所有元素都是金属 |
| B、第三、四、五、六周期元素的数目分别是8、18、32、32 |
| C、由左至右第2到12列,共十一列元素中没有非金属元素 |
| D、只有第ⅡA族元素的原子最外层有2个电子 |
下列关于常见有机化合物的说法中,不正确的是( )
| A、用溴水可鉴别苯与乙醇 |
| B、分子式为C5H12的有机物只有三种,它们互为同系物 |
| C、苯不能使溴的四氯化碳溶液褪色,说明苯分子中没有碳碳双键 |
| D、不能用KMnO4溶液除去乙烷中的乙烯 |
下列基本实验操作中,正确的是( )
A、 气体除杂 |
B、 收集氧气 |
C、 稀释溶液 |
D、 稀释溶液 |
不考虑所加溶剂对植物种子是否有害,下列物质中,不能用来提取植物种子里的油的是( )
| A、水 | B、汽油 | C、苯 | D、四氯化碳 |
重铬酸铵(NH4)2Cr2O7是一种受热易分解的盐,下列各组对重铬酸铵受热分解产物的判断,可能符合事实的是( )
①CrO3+NH3+H2O
②Cr2O3+NH3+H2O
③CrO3+N2+H2O
④Cr2O3+N2+H2O.
①CrO3+NH3+H2O
②Cr2O3+NH3+H2O
③CrO3+N2+H2O
④Cr2O3+N2+H2O.
| A、①② | B、②③ | C、①③ | D、①④ |
16O和18O是氧元素的两种原子,NA表示阿伏伽德罗常数,下列说法正确的是( )
| A、16O2与18O2互为同素异形体 |
| B、16O与18O核外电子排布方式不同 |
| C、通过化学变化可以实现16O与18O间的相互转化 |
| D、标准状况下,1.12 L16O2和1.12 L18O2均含有0.1NA个氧原子 |
下列离子方程式不正确的是( )
| A、向Ba(OH)2溶液中滴加NH4HSO4溶液刚好沉淀完全:Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3?H2O+H2O |
| B、向Ca(HCO3)2溶液中加入少量Ca(OH)2溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O |
| C、在NaOH溶液中通入少量的SO2气体:SO2+OH-=HSO3- |
| D、二氧化硅和氢氧化钠溶液反应:SiO2+2OH-=SiO32-+H2O |
 短周期元素X、Y、Z的位置如图所示,已知Y、Z两元素原子序数之和是X原子序数的4倍.X、Y、Z三元素的元素符号是( )
短周期元素X、Y、Z的位置如图所示,已知Y、Z两元素原子序数之和是X原子序数的4倍.X、Y、Z三元素的元素符号是( )| A、N、Si、S |
| B、O、P、C1 |
| C、F、S、Ar |
| D、C、A1、P |