题目内容
4.鉴别NaCl、NaBr、NaI三种溶液可以选用的试剂是( )| A. | 碘水、淀粉溶液 | B. | 溴水、汽油 | ||
| C. | 氯水、四氯化碳 | D. | 硝酸银溶液、稀硝酸 |
分析 鉴别NaCl、NaBr、NaI,可根据阴离子的性质不同以及氧化性强弱Cl2>Br2>I2判断反应的可能性,并结合萃取现象及卤化银沉淀的颜色进行检验.
解答 解:A.均不与碘水反应,现象相同,不能鉴别,故A错误;
B.只有NaI与溴水反应,不能鉴别NaCl、NaBr,故B错误;
C.氯水与NaBr、NaI反应分别生成溴、碘,则再加四氯化碳,出现不同现象,分别为分层后下层橙红色、分层后下层为褐色,现象不同,可鉴别,故C正确;
D.分别生成AgCl、AgBr、AgI沉淀,现象分别为白色、浅黄色、黄色,可鉴别,故D正确.
故选CD.
点评 本题考查物质的鉴别,为高频考点,侧重物质性质及性质差异的考查,把握氧化性的强弱及反应中的不同现象为解答的关键,侧重氧化还原及萃取现象的考查,题目难度不大.

练习册系列答案
相关题目
9.下列说法正确的是( )
| A. | 同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H相同 | |
| B. | 任何酸与碱发生中和反应生成1 mol H2O的过程中,能量变化均相同 | |
| C. | 已知:①2H2(g)+O2(g)═2H2O(g)△H1②2H2(g)+O2(g)=2H2O(1)△H2,则△H1<△2 | |
| D. | 已知:①C(s,石墨)+O2(g)═CO2(g)△H=-393.5kJ•mol-1,②C(s,金刚石)+O2(g)═CO2(g)△H=-395.0 kJ•mol-1 则C(s,石墨)=C(s,金刚石)△H=-1.5 kJ•mol-1 |
16.下列离子方程式正确的是( )
| A. | 亚硫酸钠溶液加入稀硝酸:SO32-+2H+=SO2↑+H2O | |
| B. | 将1mol•L-1 NaAlO2溶液和1.5mol•L-1的HCl溶液等体积互相均匀混合:6AlO2-+9H++3H2O=5Al(OH)3↓+Al3+ | |
| C. | 向Al2(SO4)3溶液中加入过量NH3•H2O:Al3++4NH3•H2O=[Al(OH)4]-+4NH4+ | |
| D. | 铵明矾[NH4Al(SO4)2•12H2O]溶液中加入过量Ba(OH)2溶液:Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O |
13.甲溶液:氨水质量分数为1%的溶液与9%的溶液等体积混合;乙溶液:硝酸质量分数为1%的溶液与9%的溶液等体积混合;丙溶液:硫酸质量分数为1%的溶液与9%的溶液等质量混合.则下列叙述正确的是( )
| A. | 甲、乙、丙溶液中溶质的质量分数均大于5% | |
| B. | 甲溶液中溶质的质量分数小于5%,乙、丙溶液中溶质的质量分数大于5% | |
| C. | 甲溶液中溶质的质量分数小于5%,乙的大于5%,丙的等于5% | |
| D. | 甲、乙、丙溶液中溶质的质量分数均等于5% |
14.中国科学家利用干冰和金属钠在不锈钢反应釜中反应合成出微米级金刚石,其反应为CO2(s)+Na$\stackrel{440℃}{→}$金刚石+石墨+Na2CO3.下列说法不正确的是( )
| A. | 金刚石与石墨互为同素异形体 | |
| B. | 11.5 g金属钠的物质的量为0.5 mol | |
| C. | 44 g CO2在标准状况下的体积为22.4 L | |
| D. | 该反应中碳元素发生了氧化反应 |
 ; B的结构简式CH3CH2CHO;B的物质的量0.06mol;
; B的结构简式CH3CH2CHO;B的物质的量0.06mol;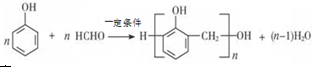 .
.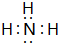 ;实验室制备气体A的化学方程式2NH4Cl+Ca(OH)2 $\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑B的水溶液不呈中性的原因NH4++H2O?NH3.H2O+H+(用离子方程式表示)
;实验室制备气体A的化学方程式2NH4Cl+Ca(OH)2 $\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑B的水溶液不呈中性的原因NH4++H2O?NH3.H2O+H+(用离子方程式表示)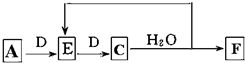
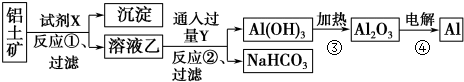
 已知:CH3CH2OH+NaBr+H2SO4(浓)$\stackrel{△}{→}$ CH3CH2Br+NaHSO4+H2O.
已知:CH3CH2OH+NaBr+H2SO4(浓)$\stackrel{△}{→}$ CH3CH2Br+NaHSO4+H2O.