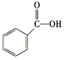
题目内容
17.溴乙烷中混有杂质乙醇,除去乙醇的方法是( )| A. | 加热蒸发 | B. | 过滤 | C. | 加水、萃取、分液 | D. | 加苯、萃取、分液 |
分析 溴乙烷与乙醇互溶,但沸点不同,但乙醇与水互溶,溴乙烷不溶于水,以此来解答.
解答 解:溴乙烷与乙醇互溶,但沸点不同,可蒸馏分离,或乙醇与水互溶,溴乙烷不溶于水,则加水、萃取、分液可除杂,
故选C.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、混合物分离方法为解答的关键,侧重分析与实验能力的考查,注意有机物性质的应用,题目难度不大.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
7. 汽车作为一种现代交通工具正在进入千家万户,汽车尾气中含有CO、NOx等有毒气体,其污染问题也成为当今社会急需解决的问题.
汽车作为一种现代交通工具正在进入千家万户,汽车尾气中含有CO、NOx等有毒气体,其污染问题也成为当今社会急需解决的问题.
(1)对汽车加装尾气净化装置,可使CO、NOx有毒气体相互反应转化为无毒气体.
2xCO+2NOx═2xCO2+N2,当转移电子物质的量为0.4x mol时,该反应生成标准状况下的N2体积2.24L.
(2)一氧化碳是一种用途相当广泛的化工基础原料.可以还原金属氧化物,还可以用来合成很多有机物如甲醇等.在压强为0.1MPa条件下,将a mol CO与3a mol H2的混合气体在催化剂作用下反应生成甲醇:CO(g)+2H2(g)?CH3OH(g)
①该反应的平衡常数表达式为$\frac{c(C{H}_{3}OH)}{c(CO){c}^{2}({H}_{2})}$.
②取一定体积CO和H2的混合气体(物质的量之比为1:2),加入恒容密闭容器中发生上述反应,反应过程中测得甲醇的体积分数φ(CH3OH)与反应温度T的关系如图1所示,则该反应的△H<0 (填“>”、“<”或“=”).
③在两种不同条件下发生反应,测得CH3OH的物质的量随时间变化如图2所示,曲线Ⅰ、Ⅱ对应的平衡常数大小关系为KⅠ>KⅡ(填“>”、“<”或“=”).
④若容器容积不变,下列措施可增加甲醇产率的是BD
A.升高温度 B.将CH3OH(g)从体系中分离
C.充入He,使体系总压强增大 D.再充入1mol CO和3mol H2
⑤经测定不同温度下该反应的平衡常数如表:
若某时刻、250℃测得该反应的反应物与生成物的浓度为c(CO)=0.4mol/L、c(H2)=0.4mol/L、c(CH3OH)=0.8mol•L-1,则此时v正<v逆(填>、<或=).
(3)甲醇是重要的基础化工原料,又是一种新型的燃料,最近有人制造了一种燃料电池,一个电极通入空气,另一个电极加入甲醇,电池的电解质是掺杂了Y2O3的ZrO2晶体,它在高温下能传导O2-离子.该电池的正极反应式为O2+4e-=2O2-.电池工作时,固体电解质里的O2-向负极移动.
 汽车作为一种现代交通工具正在进入千家万户,汽车尾气中含有CO、NOx等有毒气体,其污染问题也成为当今社会急需解决的问题.
汽车作为一种现代交通工具正在进入千家万户,汽车尾气中含有CO、NOx等有毒气体,其污染问题也成为当今社会急需解决的问题.(1)对汽车加装尾气净化装置,可使CO、NOx有毒气体相互反应转化为无毒气体.
2xCO+2NOx═2xCO2+N2,当转移电子物质的量为0.4x mol时,该反应生成标准状况下的N2体积2.24L.
(2)一氧化碳是一种用途相当广泛的化工基础原料.可以还原金属氧化物,还可以用来合成很多有机物如甲醇等.在压强为0.1MPa条件下,将a mol CO与3a mol H2的混合气体在催化剂作用下反应生成甲醇:CO(g)+2H2(g)?CH3OH(g)
①该反应的平衡常数表达式为$\frac{c(C{H}_{3}OH)}{c(CO){c}^{2}({H}_{2})}$.
②取一定体积CO和H2的混合气体(物质的量之比为1:2),加入恒容密闭容器中发生上述反应,反应过程中测得甲醇的体积分数φ(CH3OH)与反应温度T的关系如图1所示,则该反应的△H<0 (填“>”、“<”或“=”).
③在两种不同条件下发生反应,测得CH3OH的物质的量随时间变化如图2所示,曲线Ⅰ、Ⅱ对应的平衡常数大小关系为KⅠ>KⅡ(填“>”、“<”或“=”).
④若容器容积不变,下列措施可增加甲醇产率的是BD
A.升高温度 B.将CH3OH(g)从体系中分离
C.充入He,使体系总压强增大 D.再充入1mol CO和3mol H2
⑤经测定不同温度下该反应的平衡常数如表:
| 温度(℃) | 250 | 300 | 350 |
| K | 2.041 | 0.270 | 0.012 |
(3)甲醇是重要的基础化工原料,又是一种新型的燃料,最近有人制造了一种燃料电池,一个电极通入空气,另一个电极加入甲醇,电池的电解质是掺杂了Y2O3的ZrO2晶体,它在高温下能传导O2-离子.该电池的正极反应式为O2+4e-=2O2-.电池工作时,固体电解质里的O2-向负极移动.
5.下列各组离子,能在溶液中大量共存的是( )
| A. | K+、H+、SO42-、OH- | B. | Na+、H+、Cl-、SO42- | ||
| C. | Na+、Ca2+、CO32-、NO3- | D. | Ba2+、Cu2+、Cl-、SO42- |
12.下列实验现象描述不正确的是( )
| 选项 | 实验 | 现象 |
| A | 加热放在坩埚中的小钠块 | 钠先熔化成光亮的小球,燃烧时,火焰为黄色,燃烧后,生成淡黄色固体 |
| B | 在酒精灯上加热铝箔 | 铝箔熔化,失去光泽,熔化的铝并不滴落,好像有一层膜兜着 |
| C | 在含有酚酞的水中加入一小块钠 | 钠浮在水面上,四处游动,发出嘶嘶响声,溶液变红 |
| D | 在空气中久置的铝条放入NaOH溶液中 | 立刻产生大量无色气泡,铝条逐渐变细,铝条逐渐发热 |
| A. | A | B. | B | C. | C | D. | D |
2.下列说法中正确的为( )
| A. | 原子得失电子能力与该原子最外层电子数多少有关 | |
| B. | ⅠA族、ⅡA族元素的阳离子与同周期稀有气体元素的原子具有相同的核外电子排布 | |
| C. | ⅦA族元素的原子随核电荷数的增加,得电子能力逐渐减弱 | |
| D. | 前三周期元素中共有非金属元素12种 |
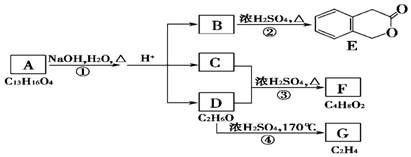
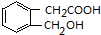
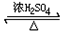
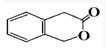 +H2O(有机物须用结构简式表示)
+H2O(有机物须用结构简式表示)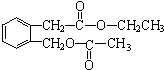 ;反应④的反应类型是消去反应.
;反应④的反应类型是消去反应. .
. .
. .预测该芳香烃能(填“能”或“不能”)发生该类反应.
.预测该芳香烃能(填“能”或“不能”)发生该类反应.
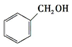 c.
c.