题目内容
下列说法正确的是( )
| A、若原子X的质子数为a,则X的质量数一定不为a |
| B、若两种元素形成的离子M2-和N+电子层结构相同,则离子半径M2->N+ |
| C、同周期非金属氧化物对应水化物酸性从左到右依次增强 |
| D、由两种元素组成的化合物,若含有离子键,就没有共价键 |
考点:原子结构与元素的性质,共价键的形成及共价键的主要类型
专题:元素周期律与元素周期表专题
分析:A.原子的质量数=质子数+中子数;
B.电子层结构相同的离子其离子半径随着原子序数增大而减小;
C.元素的非金属性越强,其最高价氧化物的水化物酸性越强,但O、F元素除外;
D.由两种元素组成的化合物,如果含有离子键,可能含有共价键.
B.电子层结构相同的离子其离子半径随着原子序数增大而减小;
C.元素的非金属性越强,其最高价氧化物的水化物酸性越强,但O、F元素除外;
D.由两种元素组成的化合物,如果含有离子键,可能含有共价键.
解答:
解:A.原子的质量数=质子数+中子数,
H原子中没有中子,所以若原子X的质子数为a,则X的质量数可能为a,故A错误;
B.电子层结构相同的离子,阳离子原子序数大于阴离子,电子层结构相同的离子,其离子半径随着原子序数增大而减小,所以离子半径M2->N+,故B正确;
C.同一周期元素,元素的非金属性随着原子序数增大而增强,元素的非金属性越强,其最高价氧化物的水化物酸性越强,但O、F元素除外,故C错误;
D.由两种元素组成的化合物,如果含有离子键,可能含有共价键,如Na2O2,故D错误;
故选B.
1 1 |
B.电子层结构相同的离子,阳离子原子序数大于阴离子,电子层结构相同的离子,其离子半径随着原子序数增大而减小,所以离子半径M2->N+,故B正确;
C.同一周期元素,元素的非金属性随着原子序数增大而增强,元素的非金属性越强,其最高价氧化物的水化物酸性越强,但O、F元素除外,故C错误;
D.由两种元素组成的化合物,如果含有离子键,可能含有共价键,如Na2O2,故D错误;
故选B.
点评:本题考查化学键、元素周期律、原子结构等知识点,侧重考查分析判断能力,采用举例法分析解答,注意规律中的特例,易错选项是AC.

练习册系列答案
相关题目
下列各种环境下的离子组合能够大量共存的是( )
| A、中性溶液中,Na+、Fe3+、SO42-、ClO- |
| B、pH=0的溶液中,Al3+、NH4+、Ca2+、SO42- |
| C、c(H+)=1.0×10-14mol?L-1的溶液中,Na+、AlO2-、S2-、SO32- |
| D、石蕊试纸变红的溶液中,Fe2+、I-、NO3-、ClO- |
下列有关物质结构的表述正确的是( )
| A、次氯酸的结构式:H-Cl-O | ||
B、中子数为20的氯原子:
| ||
C、四氯化碳的电子式: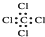 | ||
D、Cl-的结构示意图: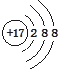 |
在25℃时,用蒸馏水稀释1mol/L的醋酸溶液至0.01mol/L,随溶液的稀释,下列说法正确的是( )
| A、溶液中所有离子浓度均减小 | ||
| B、pH的变化值等于2 | ||
C、溶液中
| ||
| D、分别与足量的Mg粉反应,0.01 mol/L的醋酸溶液产生的氢气较少 |
下列元素中,原子核外最外层电子数等于元素在周期表中的周期数的整数倍的是( )
| A、O | B、F | C、S | D、Cl |
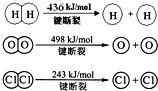

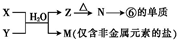
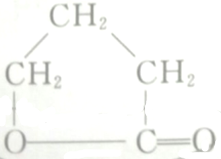 的各步反应方程式(必要的无机试剂自选,可不填满,也可补充).
的各步反应方程式(必要的无机试剂自选,可不填满,也可补充).