题目内容
10.生物材料衍生物2,5-呋喃二甲酸(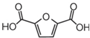 )可以替代化石燃料衍生物对苯二甲酸,与乙二醇合成材料聚2,5-呋喃二甲酸乙二醇酯(PEF).下列说法正确的是( )
)可以替代化石燃料衍生物对苯二甲酸,与乙二醇合成材料聚2,5-呋喃二甲酸乙二醇酯(PEF).下列说法正确的是( )| A. | 合成PEF的反应为加聚反应 | |
| B. | PEF不能与氢气发生加成反应 | |
| C. | 聚对苯二甲酸乙二醇酯的结构简式为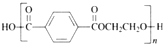 | |
| D. | 通过红外光谱法测定PEF的平均相对分子质量,可得其聚合度 |
分析 A.2,5-呋喃二甲酸和乙二醇发生反应时除了生成PEF外还生成水;
B.碳碳双键能和氢气在一定条件下发生加成反应;
C.聚对苯二甲酸乙二醇酯是由对苯二甲酸和乙二醇发生缩聚反应生成的酯;
D.红外光谱获得分子中含有何种化学键或官能团的信息.
解答 解:A.2,5-呋喃二甲酸和乙二醇发生反应时除了生成PEF外还生成水,属于缩聚反应,故A错误;
B.PEF中含有碳碳双键,能和氢气在一定条件下发生加成反应,故B错误;
C.聚对苯二甲酸乙二醇酯是由对苯二甲酸和乙二醇发生缩聚反应生成的酯,其结构简式为 ,故C正确;
,故C正确;
D.红外光谱获得分子中含有何种化学键或官能团的信息,质谱仪能记录分子离子、碎片离子的相对质量,故D错误;
故选C.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系是解本题关键,涉及反应类型判断、结构简式的书写,易错选项是D.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.分子式为C7H6O2的芳香族化合物的数目有( )
| A. | 2种 | B. | 3种 | C. | 4 | D. | 5种 |
18.已知:2CO(g)+O2(g)=2CO2(g)△H=-566kJ/mol
Na2O2(s)+CO2(g)=Na2CO3(s)+$\frac{1}{2}$O2(g)△H=-226kJ/mol
下列说法正确的是( )
Na2O2(s)+CO2(g)=Na2CO3(s)+$\frac{1}{2}$O2(g)△H=-226kJ/mol
下列说法正确的是( )
| A. | 1molCO(g)完全燃烧生成CO2(g)放出热量283J | |
| B. | 1molCO(g)完全燃烧比1molC(s)完全燃烧放出的热量多 | |
| C. | 2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2 (g)△H<-452kJ/mol | |
| D. | 当Na2O2(s)与CO2(g)反应生成Na2CO3(s)和O2 (g)放出452kJ热量时,转移的电子数为2mol |
5.S-诱抗素可保证盆栽鲜花盛开,其分子结构如图,下列说法正确的是( )
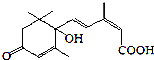

| A. | 该物质的分子式为C15H22O4 | |
| B. | 该物质环上的二氯代物共有3种 | |
| C. | 1mol该物质最多能与2 mol NaOH完全反应 | |
| D. | 该物质能发生取代、加成、氧化等反应 |
15.东汉《周易参同契》中记载:“胡粉投火中,色坏还为铅”,实验表明胡粉难溶于水,加强热产生能使澄清的石灰水变浑浊的湿气.则胡粉的主要成分为( )
| A. | PbCO3 | B. | 2PbCO3•Pb(OH)2 | C. | Pb(OH)2 | D. | (CH3COO)2Pb |
2.下列说法正确的是( )
| A. | 蔗糖在人体内水解的最终产物是葡萄糖 | |
| B. | 蔬菜水果属于碱性食物,对人体健康有益 | |
| C. | 为了防止蛋白质发生盐析,疫苗等生物制剂要冷藏 | |
| D. | 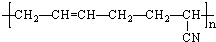 由CH2=CH2与CH2=CH-CN加聚而成 由CH2=CH2与CH2=CH-CN加聚而成 |
20.化合物CBDA的结构简式如图所示,下列说法正确的是( )
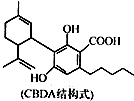

| A. | 1个CBDA分子中含有2个手性碳原子 | |
| B. | 1 mol CBDA 最多可与2molBr2反应 | |
| C. | 1 mol CBDA最多可与3 mol NaHCO3反应 | |
| D. | 1 mol CBDA最多可与2mol H2发生加成反应 |
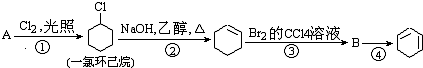
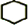 ,名称是环己烷.
,名称是环己烷. +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$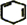 +2NaBr+2H2O.
+2NaBr+2H2O.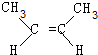 、
、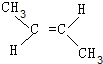 .
.
 Al(OH)3
Al(OH)3 AlO2-+H++H2O,加入NaOH溶液,H+被中和,浓度减低,Al(OH)3不断溶解.
AlO2-+H++H2O,加入NaOH溶液,H+被中和,浓度减低,Al(OH)3不断溶解.