题目内容
已知H—H键能为436 KJ/mol,H—N键能为391KJ/mol,根据化学方程式:N2 + 3H2 = 2NH3
ΔH=—92.4 KJ/mol,则N≡N键的键能是
A.431 KJ/mol B.946 KJ/mol C.649 KJ/mol D.869 KJ/mol
B
【解析】
试题分析:反应热就是断键吸收的热量与成键所释放的能量的差,N≡N+3mol×436 KJ/mol-6mol×391KJ/mol=—92.4 KJ/mol,解得N≡N的键能数值是945.6 KJ/mol,因此选项是B。
考点:考查化学反应过程中的键能与反应热的关系的知识。

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
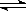 N2O4(g) 达到平衡时,再向容器内通入一定量的NO2(g),重新达到平衡后,与第一次平衡时相比,NO2的体积分数( )
N2O4(g) 达到平衡时,再向容器内通入一定量的NO2(g),重新达到平衡后,与第一次平衡时相比,NO2的体积分数( )