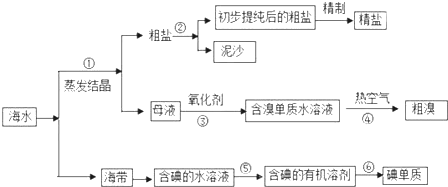
题目内容
4.氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业,它不溶于H2SO4、HNO3和醇,微溶于水,可溶于浓盐酸和氨水,在潮湿空气中易水解氧化成绿色的碱式氯化铜(Cu2(OH)3Cl).以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺过程如下: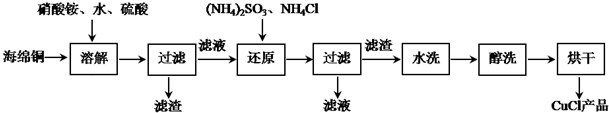
(1)写出溶解过程中发生的氧化还原反应的离子方程式:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O.
(2)还原过程中发生的主要反应的离子方程式:2Cu2++SO32-+2Cl-+H2O═2CuCl↓+SO42-+2H+.
(3)析出的CuCl晶体水洗后要立即用无水乙醇洗涤,在真空干燥机内于70℃干燥2h,冷却密封包装.70℃真空干燥、密封包装的原因是加快乙醇和水的挥发,防止CuCl在潮湿空气中水解氧化.
(4)从第二次过滤后的滤液中可回收的主要物质是(NH4)2SO4 (或者(NH4)2SO4、H2SO4)(写化学式).
(5)已知CuOH不稳定,易分解为Cu2O,298K时,CuOH的Ksp=1.0×10-14,CuCl的Ksp=1.2×10-6,把CuCl固体和NaOH溶液混合,加热,得到红色沉淀,该沉淀的化学式为Cu2O.
(6)以碳棒为电极电解CuCl2溶液也可得到CuCl,写出电解时阴极上发生的电极反应式Cu2++e-+Cl-=CuCl↓.
分析 海绵铜加入硫酸和硝酸铵溶解得到溶液主要是硫酸铜,硫酸铵等,加入亚硫酸铵还原硫酸铜、加入氯化铵氯化发生反应2CuSO4+(NH4)2SO3+2NH4Cl+H2O=2CuCl↓+2(NH4)2SO4+H2SO4,过滤得到固体为CuCl,滤液主要是硫酸铵和硫酸,结合相关物质的性质以及题目要求解答该题.
解答 解:海绵铜加入硫酸和硝酸铵溶解得到溶液主要是硫酸铜,硫酸铵等,加入亚硫酸铵还原硫酸铜、加入氯化铵氯化发生反应2CuSO4+(NH4)2SO3+2NH4Cl+H2O=2CuCl↓+2(NH4)2SO4+H2SO4,过滤得到固体为CuCl,滤液主要是硫酸铵和硫酸,
(1)铜和硝酸根离子反应的离子方程式为3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O,故答案为:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O;
(2)还原步骤发生反应的离子方程式为2Cu2++SO32-+2Cl-+H2O═2CuCl↓+SO42-+2H+,故答案为:2Cu2++SO32-+2Cl-+H2O═2CuCl↓+SO42-+2H+;
(3)70℃真空干燥、密封包装的原因是加快乙醇和水的挥发,防止CuCl在潮湿空气中水解氧化,故答案为:加快乙醇和水的挥发,防止CuCl在潮湿空气中水解氧化;
(4)由以上分析可知第二次过滤的滤液主要是硫酸铵和硫酸,故答案为:(NH4)2SO4 (或者(NH4)2SO4、H2SO4);
(5)根据题意知,氯化亚铜的溶度积大于氢氧化亚铜的溶度积,溶度积大的物质向溶度积小的物质转化,所以把CuCl固体和NaOH溶液混合,氯化亚铜和氢氧化钠反应生成氢氧化亚铜,加热时,氢氧化亚铜分解生成氧化亚铜沉淀.
故答案为:Cu2O;
(6)以碳棒为电极电解CuCl2溶液也可得到CuCl,铜离子在阴极发生还原反应生成CuCl,反应的电极方程式为Cu2++e-+Cl-=CuCl↓,故答案为:Cu2++e-+Cl-=CuCl↓.
点评 本题考查混合物分离提纯,为高频考点,把握流程中的反应、物质的性质、离子反应的书写等为解答的关键,侧重分析与应用能力的考查,题目难度不大.

 名校课堂系列答案
名校课堂系列答案| NaCl | NaHCO3 | NH4Cl | |
| 10℃ | 35.8 | 8.15 | 33.0 |
| 45℃ | 37.0 | 14.0 | 50.0 |
(1)117g食盐理论上可以制取纯碱106 g;
(2)45℃反应完毕后,有晶体析出,计算析出晶体的质量.
(3)过滤除去析出的晶体后再降温至10℃,又有晶体析出,计算所析出晶体的质量.
| A. | α1<α2<α3<α4 | B. | α3<α2<α1<α4 | C. | α2=α3<α4<α1 | D. | α2=α3<α1<α4 |
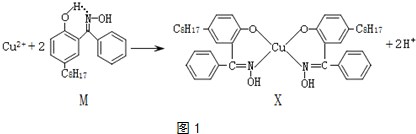
(1)X难溶于水、易溶于有机溶剂,其晶体类型为分子晶体.
(2)X中以sp2杂化、sp3杂化的原子的第一电离能由大到小顺序为N>O>C.
(3)上述反应中断裂和生成的化学键有be(填序号).
a.离子键 b.配位键 c.金属键 d.范德华力 e.共价键
(4)M与W(分子结构如图2)相比,M的水溶性小,更利于Cu2+的萃取.M水溶性小的主要原因是M能形成分子内氢键,使溶解度减小.
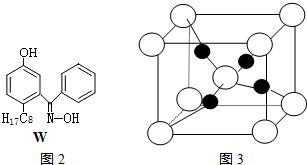
(5)硫酸铜晶体,俗称蓝矾、胆矾,具有催吐,祛腐,解毒等功效.取5.0g胆矾样品逐渐升高温度使其分解,分解过程的热重如下表.回答下列问题:
| 温度范围/℃ | 固体质量/g |
| 258~680 | 3.20 |
| 680~1000 | 1.60 |
| 1000以上 | 1.44 |
①该温度是1000℃以上.
②铜原子的配位数是4.
| A. | KMnO4溶液 | B. | NaOH溶液 | C. | 溴水 | D. | FeCl3溶液 |
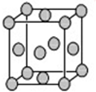 某配位化合物为深蓝色晶体,由原子序数依次增大的A、B、C、D、E五种元素组成,其原子个数比为l4:4:5:1:1. 其中C、D元素同主族且原子序数D为C的二倍,E元素的外围电子排布为(n-l)dn+6ns1,回答下列问题.
某配位化合物为深蓝色晶体,由原子序数依次增大的A、B、C、D、E五种元素组成,其原子个数比为l4:4:5:1:1. 其中C、D元素同主族且原子序数D为C的二倍,E元素的外围电子排布为(n-l)dn+6ns1,回答下列问题. .填出:E原子的核外有29 种不同运动状态的电子,B和C的第一电离能大小关系N>O (用元素符号表示).
.填出:E原子的核外有29 种不同运动状态的电子,B和C的第一电离能大小关系N>O (用元素符号表示).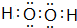 ,两种化合物可任意比互溶,解释其主要原因为H2O与H2O2之间形成氢键.
,两种化合物可任意比互溶,解释其主要原因为H2O与H2O2之间形成氢键.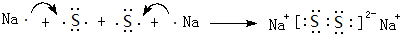 .
.