题目内容
(1)一定条件下Fe(OH)3与KClO在KOH溶液中反应可制得K2FeO4,该反应的化学方程式为 ;生成0.1molK2FeO4转移的电子的物质的量 mol.
(2)高铁电池是一种新型二次电池,电解液为碱溶液,其反应式为:
3Zn+2K2FeO4+8H2O
3Zn(OH)2+2Fe(OH)3+4KOH
放电时电池的负极反应式为 .充电时电解液的pH (填“增大”“不变”或“减小”).
(2)高铁电池是一种新型二次电池,电解液为碱溶液,其反应式为:
3Zn+2K2FeO4+8H2O
| 放电 |
| 充电 |
放电时电池的负极反应式为
考点:原电池和电解池的工作原理,铁的氧化物和氢氧化物
专题:电化学专题,元素及其化合物
分析:(1)Fe(OH)3与KClO在KOH溶液中反应可制得K2FeO4,Fe元素的化合价升高,则Cl元素的化合价降低,还生成KCl,同时生成水,结合元素的化合价变化计算转移电子数;
(2)Zn元素的化合价升高,放电时负极上Zn失去电子;由电池反应可知,充电时消耗KOH.
(2)Zn元素的化合价升高,放电时负极上Zn失去电子;由电池反应可知,充电时消耗KOH.
解答:
解:(1)Fe(OH)3与KClO在KOH溶液中反应可制得K2FeO4,Fe元素的化合价升高,则Cl元素的化合价降低,还生成KCl,同时生成水,该反应为2Fe(OH)3+3KClO+4KOH═2K2FeO4+3KCl+5H2O,由Fe元素的化合价变化可知,生成0.1molK2FeO4转移的电子的物质的量为0.1mol×(6-3)=0.3mol,
故答案为:2Fe(OH)3+3KClO+4KOH═2K2FeO4+3KCl+5H2O;0.3;
(2)Zn元素的化合价升高,放电时负极上Zn失去电子,电极反应为Zn+2OH--2e-═Zn(OH)2,由电池反应可知,充电时消耗KOH,则pH减小,
故答案为:Zn+2OH--2e-═Zn(OH)2;减小.
故答案为:2Fe(OH)3+3KClO+4KOH═2K2FeO4+3KCl+5H2O;0.3;
(2)Zn元素的化合价升高,放电时负极上Zn失去电子,电极反应为Zn+2OH--2e-═Zn(OH)2,由电池反应可知,充电时消耗KOH,则pH减小,
故答案为:Zn+2OH--2e-═Zn(OH)2;减小.
点评:本题考查氧化还原反应及原电池原理,为高频考点,把握反应中元素的化合价变化及发生的氧化反应为解答的关键,注意原电池与氧化还原反应的关系,题目难度不大.

练习册系列答案
相关题目
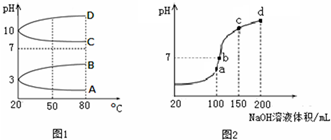
 如图是一水溶液在pH从0到14的范围内,H2CO3、HCO3-、CO32-三种成分平衡时的组成分数,下列叙述正确的是( )
如图是一水溶液在pH从0到14的范围内,H2CO3、HCO3-、CO32-三种成分平衡时的组成分数,下列叙述正确的是( )| A、此图是1.0mol/L碳酸钠溶液滴定1.0mol/L HCl溶液的滴定曲线 |
| B、在pH为6.37及10.25时,溶液中c(H2CO3)=c(HCO3-)=c(CO32-) |
| C、人体血液的pH约为7.4,则CO2在血液中多以HCO3-的形式存在 |
| D、若用CO2和NaOH反应制取Na2CO3,溶液的pH必须控制在12以上 |
下列反应的离子方程式书写正确的是( )
| A、NaAlO2溶液中通入少量CO2:2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- |
| B、向FeBr2溶液中滴加足量的氯水:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- |
| C、向40mL、8mol/L的硝酸溶液中加入5.6 g铁粉:Fe+4H++NO3-═Fe3++NO↑+2H2O |
| D、Mg(HCO3)2溶液中加入过量石灰水:Mg2++2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+MgCO3↓ |
下列装置或操作能达到所注明的实验能达到实验目的是( )
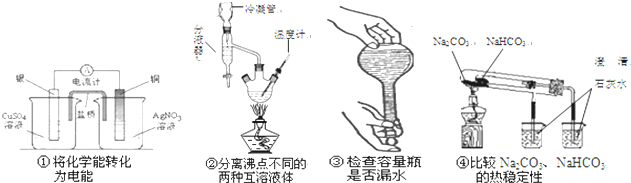

| A、①② | B、③④ | C、①③ | D、②④ |
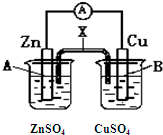 某电化学装置如图所示,下列说法正确的是( )
某电化学装置如图所示,下列说法正确的是( )| A、若X是盐桥,则电子由B电极经外电路流向A电极 |
| B、若X是盐桥,取出X电流表指针仍然偏转 |
| C、若X是锌条,则A电极的质量会减少 |
| D、若X是铜条,则A电极的电极反应式是:Zn2++2e-=Zn |
下列涉及有机物的性质或应用的说法,不正确的是( )
| A、石油的裂解为深度裂化,产物主要为乙烯等小分子烃 |
| B、油脂“硬化”后性质变的更稳定 |
| C、蔗糖、淀粉、纤维素均会水解,反应后的产物相同 |
| D、2CH3CH2OH+O2→2CH3CHO+2H2O属于氧化反应 |

 M、N、O、P、Q是元素周期表中原子序数依次递增的前四周期元素.M原子最外层电子数为内层电子数的3倍;N的焰色反应呈黄色;O的氢化物是一种强酸,其浓溶液可与M、Q的化合物反应生成O的单质;P是一种金属元素,其基态原子中有6个未成对电子.请回答下列问题:
M、N、O、P、Q是元素周期表中原子序数依次递增的前四周期元素.M原子最外层电子数为内层电子数的3倍;N的焰色反应呈黄色;O的氢化物是一种强酸,其浓溶液可与M、Q的化合物反应生成O的单质;P是一种金属元素,其基态原子中有6个未成对电子.请回答下列问题: