题目内容
16.(1)向FeCl2和KSCN的混合溶液中加入氯水,现象是溶液变红,离子方程式是2Fe2++Cl2=2Fe3++2Cl-Fe3++3SCN-=Fe(SCN)3.(2)向AgNO3溶液中加入氯水,现象是产生白色沉淀,反应的离子方程式是Ag++Cl-=AgCl↓.
(3)向氯水中滴加石蕊试液,溶液变红,起作用的微粒是H+,后又褪色,起作用的微粒是HClO.
分析 (1)向FeCl2和KSCN的混合溶液中加入氯水,氯气具有氧化性能氧化氯化亚铁为氯化铁,铁离子结合硫氰酸根离子形成血红色溶液;
(2)向AgNO3溶液中加入氯水,氯水中的氯离子结合银离子生成白色沉淀;
(3)氯气和水反应生成盐酸和次氯酸;
解答 解:(1)向FeCl2和KSCN的混合溶液中加入氯水,氯气具有氧化性能氧化氯化亚铁为氯化铁,反应的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-,铁离子结合硫氰酸根离子形成血红色溶液,反应的离子方程式为:Fe3++3SCN-=Fe(SCN)3,
故答案为:溶液变红;2Fe2++Cl2=2Fe3++2Cl-,Fe3++3SCN-=Fe(SCN)3;
(2)向AgNO3溶液中加入氯水,氯水中的氯离子结合银离子生成白色沉淀,反应的离子方程式为:Ag++Cl-=AgCl↓,
故答案为:产生白色沉淀;Ag++Cl-=AgCl↓;
(3)氯气和水反应生成盐酸和次氯酸,盐酸具有酸性,氯水具有漂白性,向氯水中滴加石蕊试液,溶液变红,起作用的微粒是H+,后又褪色,起作用的微粒是HClO,
故答案为:H+;HClO.
点评 本题考查了氯气及其化合物性质的分析判断,主要是氯水成分中各微粒的作用分析判断,注意次氯酸的漂白性,题目较简单.

练习册系列答案
相关题目
6.下列各组混合物中,能用分液漏斗进行分离的是( )
| A. | 酒精和水 | B. | 碘和酒精 | C. | 水和CCl4 | D. | 汽油和植物油 |
7.下列离子方程式书写正确的是 ( )
| A. | Ca(HCO3)2溶液中加入少量NaOH溶液:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O | |
| B. | 向NaClO溶液中通入少量SO2:2ClO-+SO2+H2O═2HClO+SO32- | |
| C. | Cl2通入水中:Cl2+H2O═2H++Cl-+ClO- | |
| D. | 向NaHSO4溶液中滴加Ba(OH)2溶液至呈中性:2H++SO42-+Ba2++2OH-═2H2O+BaSO4↓ |
4.为了探究FeS04和Cu(N03)2的混合物中各组分的含量,现设计如下流程.下列叙述中错误的是( ) 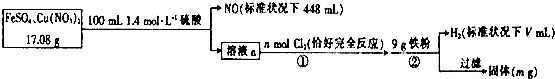

| A. | V=2240 | |
| B. | n=0.02 | |
| C. | 原混合物中FeS04的质量分数约为89% | |
| D. | m=0.6 |
11.为鉴别K2CO3和NaHCO3两种白色固体,有4位同学分别设计了不同的方法,其中不可行的是( )
| A. | 将少量的两种白色固体分别加入1 mol/L的盐酸中,看有无气泡产生 | |
| B. | 分别取样在试管中加热,将可能产生的气体通入澄清石灰水,观察有无白色浑浊 | |
| C. | 分别取样配成溶液,滴加BaCl2溶液,观察有无白色沉淀 | |
| D. | 分别配成溶液,用铂丝蘸取溶液在酒精灯火焰上灼烧,观察火焰的颜色 |
1.下列实验操作中正确的是( )
| A. | 蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 | |
| B. | 分液操作时,先将分液漏斗中下层液体从下口放出,再将上层液体从下口放出 | |
| C. | 萃取操作时,可以选用CCl4或酒精作为萃取剂从溴水中萃取溴 | |
| D. | 蒸馏操作时,应向蒸馏液体中加入几块沸石,以防止暴沸 |
8.电子工业制造光电管时,需要一种强光照射就失电子,从而接通电路的材料,制造该材料的物质是( )
| A. | 放射元素 | B. | ⅦA族元素 | C. | 卤化银 | D. | ⅠA族元素 |
5.A、B、X、Y、Z、W六种短周期主族元素,A是地壳中含量最多的金属元素,短周期主族元素中B的原子半径最大,X、Y、Z、W元素在周期表中的相对位置如图所示,其中Z元素原子最外层电子数是电子层数的2倍.请回答下列问题:
(1)W的最高价氧化物化学式是Cl2O7;Z 的原子结构示意图为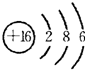 .
.
(2)A、B各自最高价氧化物对应的水化物反应的化学方程式为Al(OH)3+NaOH═NaAlO2+2H2O.
(3)AW3可用于净水,其原理是Al3++3H2O?Al(OH)3(胶体)+3H+.(请用离子方程式表示)
(4)工业合成X的简单气态氢化物是放热反应.下列措施中既能提高反应速率,又能提高原料转化率的是d.
a.升高温度 b.加入催化剂
c.将 X的简单气态氢化物及时移离 d.增大反应体系的压强
(5)标准状况下,2.24 L X的简单气态氢化物被200 mL 1 mol•L-1 X的最高价氧化物对应的水化物溶液吸收后,所得溶液中离子浓度从大到小的顺序是(用离子符号表示)c(NO3-)>c(H+)>c(NH4+)>c(OH-).
(6)WY2在杀菌消毒的同时,可将剧毒氰化物氧化成无毒气体而除去,写出用 WY2(沸点9.9℃)氧化除去CN-的离子方程式2ClO2+2CN-═N2+2CO2+2Cl-.
| X | Y | |
| Z | W |
 .
.(2)A、B各自最高价氧化物对应的水化物反应的化学方程式为Al(OH)3+NaOH═NaAlO2+2H2O.
(3)AW3可用于净水,其原理是Al3++3H2O?Al(OH)3(胶体)+3H+.(请用离子方程式表示)
(4)工业合成X的简单气态氢化物是放热反应.下列措施中既能提高反应速率,又能提高原料转化率的是d.
a.升高温度 b.加入催化剂
c.将 X的简单气态氢化物及时移离 d.增大反应体系的压强
(5)标准状况下,2.24 L X的简单气态氢化物被200 mL 1 mol•L-1 X的最高价氧化物对应的水化物溶液吸收后,所得溶液中离子浓度从大到小的顺序是(用离子符号表示)c(NO3-)>c(H+)>c(NH4+)>c(OH-).
(6)WY2在杀菌消毒的同时,可将剧毒氰化物氧化成无毒气体而除去,写出用 WY2(沸点9.9℃)氧化除去CN-的离子方程式2ClO2+2CN-═N2+2CO2+2Cl-.
6.下列溶液中Cl-的物质的量最大的是( )
| A. | 10 mL 0.1 mol•L-1的AlCl3溶液 | B. | 20 mL 0.1 mol•L-1的CaCl2溶液 | ||
| C. | 30 mL 0.2 mol•L-1的KCl溶液 | D. | 100 mL 0.25 mol•L-1的NaCl溶液 |