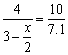题目内容
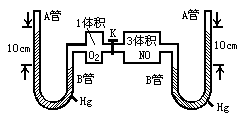
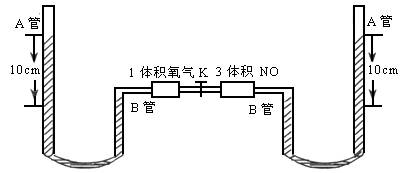
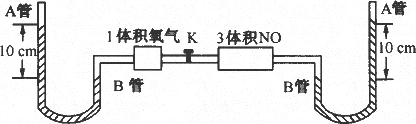
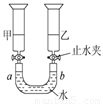
如图所示,打开两个容器间的活塞K,使两种气体混合,充分反应后,平衡状态时(温度不变),A管中汞液面比B管中汞液面高7.1cm(反应刚开始时液面高10cm),设此温度时产物为气态,汞蒸气压强忽略不计,体系容积为定值,A管上端玻璃管为真空,求NO2转化为N2O4的转化率?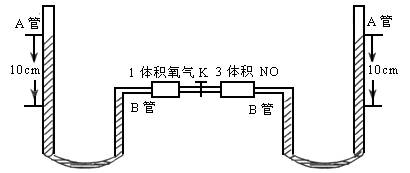
答案:
解析:
解析:
| 解:由题知,开始时两容器中O2和NO的压强相同,同温下由阿伏加德罗定律知O2和NO的物质的量之比为1∶3,设开始时O2和NO的物质的量分别为1mol和3mol。打开活塞K后,由2NO+O2══2NO2知生成2mol NO2,余1mol NO,同时发生反应2NO2ƒN2O4,又设有xmol的NO2转化为N2O4,则:
2NO2ƒN2O4 起始/mol 2 0 转化/mol x 平衡/mol (2-x) 平衡时气体总量:n(NO)+n(NO2)+n(N2O4) =[1+(2-x)+ 由图知平衡后混合气体的压强为7.1cm
Hg,由阿伏加德罗定律推出同温、同体积 x=0.32(mol) NO2的转化率为
|

练习册系列答案
相关题目